4.1.
Методы контроля. Химические факторы
Методические
указания
МУК 4.1.1090-02
"ОПРЕДЕЛЕНИЕ ЙОДА В ВОДЕ"
(утв.
Главным государственным санитарным врачом РФ
- Первым заместителем Министра здравоохранения РФ
4 января 2002 г.)
Дата введения 1 марта 2002 г.
Введены впервые
Методические указания по контролю йода в воде предназначены
для центров Госсанэпиднадзора, санитарных лабораторий промышленных предприятий,
лабораторий научно-исследовательских институтов, работающих в области гигиены
окружающей среды. Методические указания разработаны с целью обеспечения
аналитического контроля йода в водных объектах (питьевой, поверхностных,
артезианских, расфасованных минеральных и др.) и оценки соответствия уровня его
содержания гигиеническому нормативу.
Йод широко распространен в природе. В незначительных
количествах он находится повсюду: в морской воде, земной коре, растительных и
животных организмах. Соединения йода содержатся в некоторых сточных водах
химической и фармацевтической промышленности. В природных водах йод содержится
преимущественно в виде йодидов. Йод относится к важнейшим биогенным элементам,
необходимым для нормального функционирования организма человека, однако в
повышенных концентрациях он представляет опасность для здоровья. В природных
водах и в процессе водоподготовки содержание йода может колебаться в пределах
от 0,005 до 1 мг/дм3. В связи с этим особую актуальность приобретает
контроль йода в воде на уровне гигиенического норматива.
Существующая фотометрическая методика определения [1] из-за недостаточной чувствительности не
позволяет контролировать содержание йода в воде на уровне предельно допустимой
концентрации (ПДК 0,125 мг/дм3). Существенным недостатком йодометрической
методики [2] является отсутствие
метрологической аттестации.
Настоящие методические указания дают возможность
устанавливать количественный титриметрический анализ водных объектов для
определения в них содержания йода в диапазоне концентраций 0,01 - 1 мг/дм3.
Метод метрологически аттестован и обеспечивает определение йода с пределом
обнаружения 0,08 ПДК.
Методические указания разработаны в соответствии с
требованиями ГОСТов Р
8.563-96, 17.0.0.02-79.
Методические указания одобрены и рекомендованы секцией по
физико-химическим методам исследования объектов окружающей среды Проблемной
комиссии "Научные основы экологии человека и гигиены окружающей
среды".
I2 Молекулярная масса - 253,84
Йод - твердое кристаллическое вещество с резким запахом.
Температура плавления - 113,7 °С, температура кипения - 182,8 °С, плотность -
4,93 г/см3. Растворяется в хлороформе, сероуглероде, спирте, эфире,
четыреххлористом углероде. В воде мало растворим (0,028 г на 100 г при 20 °С).
Йод обладает раздражающим действием. Предельно допустимая
концентрация в воде (ПДК) - 0,125 мг/дм3.
Методика обеспечивает выполнение измерений с погрешностью,
не превышающей - 30 %, при доверительной вероятности 0,95.
Измерение концентрации йода основано на окислении йодидов до
йодатов в кислой среде бромной водой с восстановлением последних до свободного
йода по формуле:
I + 3Br2 + 3H2O → IO3
+ 6Н+ + 6Br;
KIO3 + 5KI + 3H2SO4 = 3I2 + 3K2SO4
+ 3H2O;
I2 + 2Na2S2O4 = Na2S4O6
+ 2NaI.
Количественное определение проводят йодометрическим
титрованием. Нижний предел измерения йода в анализируемой пробе 10 мкг. Определению
не мешают другие галогены.
|
Весы лабораторные ВЛА-200г-М 2-го
класса точности с погрешностью 0,02 г
|
ГОСТ 24108-88Е
|
|
Меры массы Г-2-2106 2 кл
|
ГОСТ 7328-2001
|
|
Пипетки градуированные
вместимостью 1, 2, 5, 10 см3
|
ГОСТ
29227-91
|
|
Колбы мерные, 1000 см3,
100 см3
|
ГОСТ
1770-74
|
|
Цилиндры мерные вместимостью 100,
1000 см3
|
ГОСТ
1770-74
|
|
Микробюретка вместимостью 5 см3
|
ГОСТ
20292-84
|
|
Термометр лабораторный шкальный
ТЛ-2
|
ГОСТ
215-73Е
|
|
Воронки делительные, ВД-3-2000
|
ГОСТ 9613-75
|
|
Чашки фарфоровые № 2, 3
|
ГОСТ
9147-73
|
|
Колбы плоскодонные, вместимостью
25, 50 см3
|
ТУ 92-891.029-91
|
|
Стаканы термостойкие вместимостью
1000 см3
|
ГОСТ
25336-82
|
|
Воронки лабораторные, стеклянные
|
ГОСТ
25336-82
|
|
Электропечь сопротивления
камерная, лабораторная, обеспечивающая поддержание заданного температурного
режима от 150 до 500 °С
|
ТУ 79-337-77
|
|
Шкаф сушильный, обеспечивающий
поддержание заданного температурного режима от 40 до 150 °С
|
ТУ 16-531-639-78
|
|
Электроплитка бытовая или горелка
газовая
|
ГОСТ
14919
|
|
Баня водяная, песочная
|
ТУ 64-1-2850
|
|
Палочки стеклянные оплавленные
|
ГОСТ
25330
|
|
Фильтры беззольные "синяя
лента", диаметром 5 или 7 см
|
ТУ 6-09-1678-86
|
|
Тальк
|
ГОСТ
19729-74
|
|
Йод
|
ГСО № 6088-91
|
|
Дистиллированная вода
|
ГОСТ 6709-72
|
|
Спирт этиловый ректификат
|
ГОСТ
5962-67
|
|
Калий йодистый, х.ч.
|
ГОСТ 4232-74
|
|
Калий углекислый (поташ)
|
ГОСТ 4221-76
|
|
Фенолфталеин
|
ГОСТ 5850-72
|
|
Кислота серная, х.ч.
|
ГОСТ 4204-72
|
|
Кислота хлороводородная, х.ч.
|
ГОСТ
3118-77
|
|
Крахмал
|
ГОСТ
10163-76
|
|
Тиосульфат натрия
|
ГОСТ
27068-86
|
|
Бром
|
ГОСТ 4109-64
|
|
Метиловый красный
|
ТУ 6-09-5169-84
|
|
Муравьиная кислота
|
ГОСТ
5848-73
|
|
Метиловый оранжевый
|
ТУ 6-09-5171-84
|
|
Хлороформ, х.ч.
|
ТУ 6-09-4263-76
|
Возможно использование других средств измерений, вспомогательного
оборудования, материалов и реактивов с метрологическими и техническими
характеристиками не ниже приведенных выше.
7.1. При работе с реактивами соблюдают требования
безопасности установленные для работ с токсичными, едкими и
легковоспламеняющимися веществами по ГОСТ
12.1.005-88.
7.2. Требования электробезопасности при работе с
электроустановками в соответствии с ГОСТ
12.1.019-79.
К выполнению измерений допускают лиц имеющих квалификацию не
ниже техника-химика и имеющих навыки работы с титрованием.
При выполнении измерений согласно ГОСТ
15150-69 соблюдают следующие условия:
- процессы приготовления растворов и подготовки проб к
анализу проводят при температуре воздуха (20 ± 5 °С); атмосферном давлении (630
- 800 мм рт.ст.) и влажности воздуха не более 80 % при 25 °С.
В комнате, где ведется определение йода, не должно быть
никаких йодсодержащих препаратов.
Все применяемые реактивы и дистиллированная вода должны быть
очищены от йода.
Перед выполнением измерений проводят следующие работы:
приготовление растворов, отбор проб.
10.1. Приготовление
растворов
Все растворы готовятся на безйодной дистиллированной воде.
Дистиллированная вода. Перегоняется в присутствии K2CO3.
Спирт ректификат. Перегоняется в присутствии K2CO3.
Серная кислота, 5 %-ный раствор. 30 см3
концентрированной H2SO4 (уд. вес 1,84) приливают
осторожно к дистиллированной воде (400 - 500 см3) в литровой колбе,
по охлаждении доводят дистиллированной водой до 1 дм3.
Бромная вода насыщенная. К 100 см3
дистиллированной воды прибавляют приблизительно 5 г жидкого брома и сильно
встряхивают, изредка приоткрывая пробку. Пользуются свежеприготовленной.
Серноватисто-кислый натрий, 0,1 Н раствор. Готовят из
фиксанала. Содержимое ампулы количественно перенести в мерную колбу, вместимостью
1000 см3 и разбавить бидистиллированной водой.
Йодистый калий. Проверяется на йод добавлением 5 % H2SO4
(2 - 3 капли) и крахмала. Пожелтевший препарат выдерживается на воздухе до
побеления.
Тальк. Обрабатывается концентрированной хлороводородной
кислотой в соотношении 1:3, промывается, высушивается и прокаливается.
Фенолфталеин, 1 %-ный спиртовой раствор. 1 г фенолфталеина
помещают в мерную колбу, вместимостью 100 см3 и доводят до метки 96
% спиртом.
Крахмал, 1 %-ный раствор. Смешивают 1 г растворимого крахмала
с 10 см3 дистиллированной воды и приливают к 90 см3
кипящей дистиллированной воды. Раствор консервируют небольшим количеством
хлороформа (1 - 2 капли).
Метиловый красный, 1 %-ный спиртовой раствор. 1 г метилового
красного помещают в мерную колбу, вместимостью 100 см3 и доводят до
метки 96 %-ным спиртом.
Метиловый оранжевый, 1 %-ный спиртовой раствор. 1 г
метилового оранжевого помещают в мерную колбу, вместимостью 100 см3
и доводят до метки 96 % спиртом.
Водный раствор K2CO3 готовят из
расчета 1 кг на 810 см3 воды. Раствор встряхивают в течение 5 минут
в делительной воронке с 10 см3 спирта и разделяют. Обработку
раствора спиртом повторяют несколько раз. Для измерений используют нижний слой.
Пробы воды объемом 0,5 - 6 дм3 отбирают в емкость
из темного стекла в соответствии с ГОСТ Р
51592-2000, ГОСТ Р 51593-2000.
Пробы хранят при охлаждении до 2 - 5 °С. Анализ - в день отбора проб.
При анализе 1 л пробы определяют содержание йодидов, начиная
с 0,01 мг/дм3. Пробы с более низким содержанием йодидов
предварительно концентрируют упариванием. Для определения отбирают такой объем
пробы, чтобы содержание в нем йода было в пределах 0,01 - 1 мг. В термостойкий
стакан помещают пробу исследуемой воды, прибавляют 10 капель 1 %-ного раствора
фенолфталеина и раствор K2CO3 до ярко красного
окрашивания, не исчезающего при помешивании. Пробу выпаривают на электрической
или газовой плите до объема 300 - 400 см3 (при объеме пробы менее
0,5 дм3 выпаривание производить в фарфоровой чашке № 3 на водяной
бане). Затем пробу переносят в фарфоровую чашку № 3, упаривают до сухого осадка
на водяной бане, просушивают в сушильном шкафу и прокаливают в электропечи при
температуре до 450 °С. Во избежание потери йода нужно следить, чтобы
температура электропечи была не выше 500 °С. Прокаливание продолжают до полного
обугливания органического вещества, не добиваясь его окончательного сгорания
(остаток может быть серым). Прокаленный остаток увлажняют водой, приготовленной
в соответствии с п. 10.1 (3 - 4 капли)
и растирают стеклянной палочкой до однородной массы. Если остаток жесткий,
прибавляют по каплям K2CO3 и растирают до получения
мягкой массы. Потом прибавляют 8 - 10 см3 спирта, приготовленного в
соответствии с п. 10.1, тщательно
размешивают и декантируют экстракт в другую чашку меньшего размера (№ 2). Если
остаток мучнистый и не отстаивается, прибавляют концентрированный раствор K2CO3
при помешивании стеклянной палочкой до тех пор, пока осадок полностью не
свернется. Экстрагирование повторяют с новой порцией спирта (8 - 10 см3).
После этого к остатку прибавляют 2 - 3 капли концентрированного раствора K2CO3,
высушивают на водяной бане, потом в сушильном шкафу и опять прокаливают в
электропечи, увлажняют водой и снова дважды экстрагируют. Спиртовые экстракты
объединяют. Таким образом, экстрагирование йода из сухого остатка производится
в 2 приема после прокаливания с предварительным прибавлением K2CO3.
Общий объем экстракта составляет ~ 40 см3.
Полученный экстракт выпаривают на водяной бане, прибавив 2
капли концентрированного раствора K2CO3. После этого
чашку просушивают в сушильном шкафу и прокаливают в электропечи. Так как в
экстракте минеральных веществ мало, в этих условиях происходит быстрое и полное
сгорание всего органического вещества. После охлаждения чашки добавляют 3 - 4
капли дистиллированной воды и опять экстрагируют небольшими порциями спирта (10
см3). Экстракт осторожно выпаривают на водяной, не сильно нагретой
бане с таким расчетом, чтобы спирт в чашке не закипел.
Внимание: Сухой остаток в чашке должен быть
бесцветным, в противном случае его смачивают несколькими каплями воды,
прибавляют 1 - 2 капли раствора K2CO3, сушат и
прокаливают снова, но уже не подвергая экстрагированию спиртом.
Бесцветный остаток растворяют в 1 - 1,5 см3
дистиллированной воды и фильтруют через воронку в коническую колбу емкостью около
25 см3. Объем фильтрата вместе с промывными водами должен составлять
около 4 см3. К фильтрату добавляют 2 капли раствора метилового
оранжевого, осторожно титруют 5 % раствором серной кислоты и добавляют еще 2 см3
титранта. Затем порциями по 20 - 25 капель приливают бромную воду до
окрашивания раствора в желтый цвет, обусловленного избытком бромной воды, и
ставят на заранее сильно разогретую песочную баню (~ 100 °С). Для равномерного
кипения к раствору прибавляют на кончике ножа щепотку талька, После того, как
раствор закипит, продолжают кипячение ровно 5 минут. Охлаждают колбу с
раствором под краном с холодной водой до температуры 25 °С. Для восстановления
брома в колбу добавляют 2 - 3 капли муравьиной кислоты и осторожно взбалтывают,
содержимое испытывают на бром по запаху через 2 минуты. Добавляют каплю
раствора метилового красного. Обесцвечивание индикатора свидетельствует о
присутствии брома, в таком случае добавляют 1 каплю муравьиной кислоты. Если
бледно-розовое окрашивание раствора не исчезает, прибавляют несколько крупинок
йодистого калия, 2 капли 1 %-ного раствора крахмала и спустя 5 минут титруют
0,001 Н раствором тиосульфата до слабо-розового окрашивания.
12.
Вычисление результатов измерений
Концентрацию йода в воде (мкг/дм3) определяют по
формуле:
С
= 1/6 × V × Т × g мкг/дм3,
где
V - объем 0,001 Н раствора тиосульфата натрия, см3;
T - титр 0,0 01 Н раствора йодата, выраженный мкг,
равный 127;
1/6 - количество йода из KIO3 при титровании (см.
уравнение реакции);
g - объем исследуемой пробы, дм3.
Для пробы объемом 1 дм3 концентрацию йода
вычисляют по формуле:
С
= V × 21,15 мкг/дм3
При объеме пробы 3 дм3 - С = V
× 7,05 мкг/дм3
За окончательный результат
измерения принимают среднее арифметическое значение результатов двух
параллельных измерений, выполняемое до первого десятичного знака. Вычисляют
среднее значение концентрации йода в воде:
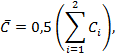
Рассчитывают относительную разницу результатов двух
параллельных измерений одной пробы:
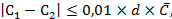
где d - оперативный контроль
сходимости, 22 %.
Средние значения результатов
измерения концентраций веществ в 2 параллельных пробах воды оформляют
протоколом по форме:
|
Протокол
№
количественного химического анализа
Дата проведения анализа
___________________________________________________
Место отбора пробы
_______________________________________________________
Название лаборатории
_____________________________________________________
Юридический адрес организации
____________________________________________
Результаты химического анализа
|
Шифр или номер пробы
|
Определяемый компонент
|
Концентрация, м кг/дм3
|
Погрешность измерения, %
|
|
|
|
|
|
Руководитель лаборатории:
Исполнитель:
|
14.1. Контроль сходимости. Выполняют по п. 12. При превышении
норматива оперативного контроля сходимости эксперимент повторяют. При повторном
превышении норматива выясняют причины, приводящие к неудовлетворительным
результатам контроля, и устраняют их.
14.2. Оперативный контроль погрешности. Проводится при смене
реактивов. Образцами для контроля являются реальные пробы питьевой и
поверхностной воды, к которым делаются добавки йода в виде растворов. Отбирают
2 пробы воды и к одной из них делают добавку таким образом, чтобы содержание
определяемого вещества увеличилось по сравнению с исходным на 50 - 150 %.
Каждую пробу анализируют в точном соответствии с прописью методики и получают
результат анализа исходной рабочей пробы - Сисх и рабочей
пробы и с добавкой С'.
Результаты анализа исходной рабочей пробы Сисх
и с добавкой С' - получают по возможности в одинаковых условиях, т.е. их
получает 1 аналитик с использованием одного набора мерной посуды, одной партии
реактивов и т.д.
Результаты контроля признаются
удовлетворительными, если выполняется условие:
|C'
- Cисх - С| < Kg, где
С - добавка вещества, мкг/дм3;
Kg - норматив оперативного контроля погрешности,
мг/дм3.
При внешнем контроле (Р =
0,95) принимают:
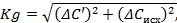
где ΔCисх и ΔС' - характеристики
погрешности измерений для исходной пробы и пробы с добавкой соответственно,
мкг/дм3.
Их вычисляют по формуле:
ΔCисх =
0,01 × δотн. × Cисх,
ΔC' = 0,01 × δотн.
× C',
При внутрилабораторном контроле (Р
= 0,90) принимают: K'g = 0,84Kg.
При превышении норматива
оперативного контроля погрешности эксперимент повторяют. При повторном
превышении указанного норматива выясняют причины, приводящие к
неудовлетворительным результатам контроля, и устраняют их.
|
Главный
государственный
санитарный врач
Российской Федерации -
Первый заместитель
Министра здравоохранения
Российской Федерации
|
Г.Г.
Онищенко
|
1. Определение концентраций химических
веществ в воде централизованных систем питьевого водоснабжения: Сборник
методических указаний. МУК 4.1.737-99 - 4.1.754-99.
2. Унифицированные методы исследования
качества вод. Методы химического анализа вод. - Ч. 1. - М., 1977. - с. 424.
3. ГОСТ
Р 8.563-96. ГСИ. "Методики выполнения измерений".
4. ГОСТ
17.0.0.02-79. "Охрана природы. Метрологическое обеспечение контроля
загрязненности атмосферы, поверхностных вод и почвы. Основные положения".
5. Питьевая вода. Гигиенические требования к
качеству воды централизованных систем питьевого водоснабжения. Контроль
качества. СанПиН
2.1.4.1074-01.
СОДЕРЖАНИЕ
Новости
Библиотека
Soft по ОТ и ПБ
Консультации
Агрегатор
Услуги
Форум
Золотой фонд
ССОТ
CHAT-OT


.webp)