4.2.
Методы контроля. биологические и микробиологические факторы
Методические
указания
МУК 4.2.2963-11
«Методические указания по лабораторной диагностике
заболеваний,
вызываемых Escherichia coli, продуцирующих шига-токсины
(STEC-культуры), и обнаружению возбудителей STEC-инфекций
в пищевых продуктах»
(утв. Главным государственным санитарным врачом РФ 19 августа 2011 г.)
Дата
введения: с момента утверждения
Введены
впервые
1.1. Методические указания определяют схемы выделения из
клинического материала и пищевых продуктов трех групп эшерихий, продуцирующих
шига-токсины, и их идентификацию: a) E. coli О104:Н4, эпидемического штамма,
вызвавшего вспышку STEC-инфекции в Германии и других странах весной 2011 года
б) E. coli О157:H7/О157:H-, основного представителя группы
энтерогеморрагических эшерихий; и в) энтерогеморрагических эшерихий, не
относящихся к серовару E. coli О157:H7»
Ключевым поражающим фактором этих трех групп эшерихий
являются шига-токсины - Stx1 и Stx2.
1.2. Методические указания предназначены для специалистов
бактериологических лабораторий учреждений Федеральной службы по надзору в сфере
защиты прав потребителей и благополучия человека и других организаций,
независимо от их организационно-правовой формы, имеющих
санитарно-эпидемиологическое заключение и лицензию на работу с микроорганизмами
I - IV групп патогенности.
В настоящих методических указаниях использованы ссылки и
положения следующих документов:
2.1. Федеральный закон «О санитарно-эпидемиологическом
благополучии населения» № 52-ФЗ
от 30 марта 1999 г.
2.2. Закон Российской Федерации от 07.02.1992 г. № 2300-I «О защите прав
потребителей».
2.3. Федеральный закон от 02.01.2000 г. № 29-ФЗ
«О качестве и безопасности пищевых продуктов».
2.4. «Положение о государственном
санитарно-эпидемиологическом нормировании», утвержденное Постановлением
Правительства Российской Федерации № 554 от 24 июля 2000 г.
2.5. Приказ Минздрава СССР от 24.04.1985 № 535 «Об
унификации микробиологических (бактериологических) методов исследования,
применяемых в клинико-диагностических лабораториях лечебно-профилактических
учреждений».
2.6. «Единые санитарно-эпидемиологические и гигиенические требования
к товарам, подлежащим санитарно-эпидемиологическому надзору (контролю)»,
утвержденные Решением Комиссии Таможенного союза от 28.05.2010 года № 299.
2.7. СанПиН
2.3.2.1078-01 «Гигиенические требования к безопасности и пищевой ценности
пищевых продуктов».
2.8. СП
1.3.1285-03 «Безопасность работы с микроорганизмами I - II групп
патогенности (опасности)».
2.9. СП
1.3.2322-08 «Безопасность работы с микроорганизмами III - IV групп
патогенности (опасности) и возбудителями паразитарных болезней и СП 1.3.2885-11
«Дополнения и изменения № 2 к СП 1.3.2322-08 «Безопасность работы с
микроорганизмами III - IV групп патогенности (опасности) и возбудителями
паразитарных болезней».
2.10. СанПиН
2.1.3.2630-10 «Санитарно-эпидемиологические требования к организациям,
осуществляющим медицинскую деятельность».
2.11. МУК
4.2.992-00 «Методы выделения и идентификации энтерогеморрагической кишечной
палочки E. coli О157:Н7».
2.12. МУК 4.2.2812-11, Москва, 2011, «Методы выявления и идентификации патогенных бактерий -
возбудителей инфекционных заболеваний с пищевым путем передачи в продуктах
питания на основе ПЦР с гибридизационно-флуоресцентной детекцией».
2.13. МУ
1.3.2569-09 «Организация работы лабораторий, использующих методы
амплификации НК при работе с материалом, содержащим микроорганизмы I - IV групп
патогенности».
2.14. Методы выявления патогенных микроорганизмов с
использованием иммунохроматографических экспресс-тестов производства Merck
(Германия): Методические рекомендации. - М.: Федеральный центр
Госсанэпиднадзора Минздрава России, 2004. - 23 с.
2.15. Методические указания «МУ № 04-723/3 от 17.12.84 г.
«По микробиологической диагностике заболеваний, вызываемых энтеробактериями».
2.16. ГОСТ
Р 52816-2007 «Продукты пищевые. Методы выявления и определения количества
бактерий группы кишечных палочек (колиформных бактерий)».
2.17. ГОСТ
Р 53430-2009 «Молоко и продукты переработки молока. Методы
микробиологического анализа».
2.18. ГОСТ
9792-73 «Колбасные изделия и продукты из свинины, баранины, говядины и мяса
других видов убойных животных и птиц».
2.19. ГОСТ 21237-75
«Мясо. Методы микробиологического анализа».
2.20. ГОСТ
4288-76 «Изделия кулинарные и полуфабрикаты из рубленного мяса. Правила
приемки и методы испытания».
2.21. ГОСТ
Р 50396.0-92 «Мясо птицы, субпродукты и полуфабрикаты птичьи. Методы отбора
проб и подготовка к микробиологическим исследованиям».
2.22. ГОСТ
7702.2.2-93 «Мясо птицы, субпродукты и полуфабрикаты птичьи. Методы
выявления и определения количества бактерий группы кишечных палочек».
2.23. ГОСТ
Р ИСО 7218-2008 «Микробиология пищевых продуктов и кормов для животных. Общие
требования и рекомендации по микробиологическим исследованиям».
3.1. Острые кишечные инфекции с проявлениями
геморрагического колита (ГК) и гемолитикоуремического синдрома (HUS),
вызываемые эшерихиями, продуцирующими шигатоксины (STEC), распространены во
многих странах мира и регистрируются в виде спорадических случаев или вспышек с
охватом больших количеств людей: от десятков до нескольких тысяч.
Среди штаммов E. coli особое значение имеют патогенные
штаммы, синтезирующие веротоксины (шигаподобные токсины). Выделяется группа
энтерогеморрагических штаммов E. coli (EHEC) с высокопатогенными сероварами
О157:Н7, О26, О103, О111, О145 и др. Продукция веротоксинов является наиболее
общим критерием для определения данной группы бактерий. Веротоксины можно
классифицировать по основным группам: веротоксины 1 (VT1, SLT1, Stx1) и
веротоксины 2 (VT2, SLT2, Stx2). Штаммы ЕНЕС способны продуцировать либо только
токсины первой (VT1) или второй группы (VT2), либо обе группы токсинов (VT1) и
(VT2) одновременно.
Резервуаром данной инфекции являются крупный рогатый скот,
козы и овцы. Загрязнение пищевых продуктов происходит в процессе их
приготовления при неудовлетворительном состоянии гигиены на производстве, а
также при недостаточной термической обработке продуктов.
3.2. Люди заболевают STEC-инфекциями после употребления
недоброкачественных мясных продуктов, непастеризованного молока, йогуртов,
сыра, овощей, шпината, разных салатов, пророщенных зерен бобовых, соков, других
пищевых продуктов и воды, обсемененных STEC-бактериями. Возможно заражение
людей при контакте с сельскохозяйственными и домашними животными, а также при
непосредственном контакте с больными STEC-инфекцией. Штаммы ЕНЕС представляют
серьезную угрозу жизни особенно для пожилых людей и детей до 5 лет.
Наиболее частый путь распространения инфекции -
фекально-оральный.
Инкубационный период при STEC-инфекции - в среднем от трех
до восьми дней.
Основными клиническими симптомами при STEC-инфекциях
являются острые абдоминальные боли, диареи, часто с кровью (геморрагический
колит), рвота, тошнота, температура может быть незначительно повышена.
Большинство заболевших выздоравливает в течение 5 - 10 дней без каких-либо
осложнений. У части больных (до 30%) спустя неделю после начала диареи может развиться
гемолитико-уремический синдром (HUS). Основные симптомы HUS - снижение частоты
мочеиспускания, чувство сильной усталости, анемия кожи и слизистых. У больных с
HUS развивается острая почечная недостаточность, гемолитическая анемия и
тромбоцитопения. Лечение больных с HUS для клиницистов является непростой
задачей, поскольку антимикробная терапия STEC-инфекций пока не разработана.
Смертность среди больных HUS высокая и колеблется от 3 до 30 %. У переболевших
людей может отмечаться непродолжительный период бактерионосительства.
3.3. Настоящие методические указания определяют алгоритм
выделения из клинического материала и пищевых продуктов и идентификации
эшерихий, продуцирующих веротоксины (шигаподобные токсины): а) серовара
О104:Н4, возбудителя эпидемической вспышки геморрагического колита и HUS в
Германии и других странах весной 2011 года; б) энтерогеморрагического серовара O157:Н7/О157:Н; и в) сероваров, «не относящихся к О157:Н7».
Выделение указанных патогенов проводят на
дифференциально-диагностических питательных средах с последующим исследованием
чистых культур в реакции латексной агглютинации (РЛА), или методом полимеразной
цепной реакции (ПЦР) с электрофоретической детекцией продуктов амплификации в
агарозном геле, или их дальнейшей идентификацией на иммунохроматографическом
тесте с применением питательного бульона для индукции синтеза веротоксинов
(содержащий индуктор синтеза веротоксинов - карбадокс).
3.4. Серовар O157:Н7/О157:Н является
доминирующим представителем энтерогеморрагической группы эшерихий, наиболее
часто вызывающих геморрагический колит и HUS у людей во многих странах мира.
Источником и основным резервуаром этого патогена являются
сельскохозяйственные животные: крупный рогатый скот, овцы, козы, свиньи и
птица, а также дикие животные. Носительство этого серовара среди
сельскохозяйственных животных в России составляет от 2 до 3 процентов.
По культурально-морфологическим свойствам штаммы серовара
O157:Н7/О157:Н - типичные представители вида E. coli, но имеют некоторые
биохимические особенности: не образует O157:Н7/О157:Н β-Д-глюкоронидазу и
не ферментирует многоатомный спирт сорбитол. Эти свойства патогена используют
при его выделения из клинического материала и пищевых продуктов.
Основными факторами патогенности серовара O157:Н7/О157:Н являются
веротоксины (шигаподобные токсины) Stx1 и Stx2 (или только Stx2), белок
интимин, ответственный за адгезию возбудителя к эпителиальным клеткам
кишечника, энтерогемолизин и жгутиковый антиген Н7. Перечисленные факторы
патогенности детерминируются соответственно генами stx1, stx2, еае, hly и flic.
Указанные гены, а также rfb гены, ответственные за синтез соматического О
антигена, являются основными генами-мишенями для диагностических
ПЦР-тест-систем, используемых при идентификации серовара E. coli O157:Н7/О157:Н.
3.5. Причиной геморрагического колита и HUS у человека,
помимо серовара O157:Н7/О157:Н, могут выступать энтерогеморрагические эшерихии
других серологических О-групп, хотя их удельный вес в структуре STEC-инфекций
значительно меньше, чем серовара O157:Н7/О157:Н. В настоящее время уже
насчитывается более 25 таких сероваров E. coli. Среди этой группы
STEC-патогенов чаще всего от больных выделяют эшерихии серогрупп О26, О111,
О55, О103, О45, О121, О113, О117 и О145.
Группа этих возбудителей, в отличие от серовара
O157:Н7/О157:Н, не имеет каких-либо фенотипических маркеров, которые можно было
бы использовать в качестве селективных при высеве анализируемых образцов на
питательные среды. Это обстоятельство значительно затрудняет выделение и
идентификацию возбудителей геморрагического колита и HUS, «не относящихся к
О157:Н7».
В геноме этой группы патогенов, как правило, обнаруживают
гены синтеза интимина - еае и гены веротоксинов (шигаподобных токсинов) - stx1
и stx2 (либо только stx1 или stx2). Поэтому реально диагностировать группу STEC
штаммов «не относящихся к О157:Н7», возможно либо только по обнаружению у них
способности продуцировать шига-токсины, либо по индикации у них генов stx1 и
stx2.
3.6. Серовар E. coli O104:H4, явившийся причиной крупной
эпидемической вспышки геморрагического колита и тяжелых случаев HUS в Германии
и других странах Европы весной - летом 2011 года, и охватившей более 4000
человек, по своим культуральным, биохимическим и другим фенотипическим
свойствам является типичным представителем вида E. coli. Однако его генотип
существенно отличается от генотипа «классического» представителя группы
энтерогеморрагических эшерихий - E. coli O157:Н7/О157:Н: он не содержит генов
интимина (еае), вероцитотоксинов (шигаподобных токсинов) 1-го типа (Stx1) и
энтерогемолизина. Его геном на 93% идентичен геному штамма E. coli 55989,
относящемуся к группе энтероаггрегативных эшерихий (ЕАЕС), возбудителей диареи
у человека, выделенному в Центральной африканской республике. Однако в отличие
от энтероаггрегативных штаммов в геноме штамма E. coli О104:Н4 присутствует ген
синтеза веротоксина (шигаподобного токсина) 2-го типа (Stx2), то есть генотип
этого высоковирулентного для человека штамма вобрал в себя факторы патогенности
энтероаггрегативных эшерихий (способность к аггрегации и образованию биопленки
на слизистой кишечника) и энтерогеморрагических (способность к синтезу
веротоксина (шигаподобного токсина) Stx2 - основного фактора, обусловливающего
HUS у человека). Кроме того, эпидемический штамм E. coli O104:H4
характеризуется широким спектром устойчивости к антибактериальным препаратам: к
бета-лактамам - ампициллину, амоксициллину/клавулонату,
пиперациллину/сульбактаму, пиперациллину/тазобактаму, цефуроксину, цефуроксиму,
цефокситину, цефотаксиму, цефтазидиму, цефподоксиму, а также к стрептомицину,
налидиксовой кислоте, тетрациклину и триметоприму/сульфаметоксазолу.
Устойчивость к бета-лактамам обусловлена присутствием в геноме штамма
бета-лактамаз расширенного спектра (БЛРС) - СТХ-М-15 и ТЕМ-1. Наличие у штамма
E. coli O104:H4 маркеров резистентности к антибиотикам может быть использовано
при его выделении из клинического материала и пищевых продуктов.
Взятие материала от клинически больных и контактных и его
доставка в лабораторию для исследования осуществляется в соответствии с МУК
4.2.992-00 «Методы выделения и идентификации энтерогеморрагической кишечной
палочки E. coli О157:Н7» и МУ № 04-723/3 от 17.12.84 г. «По микробиологической
диагностике заболеваний, вызываемых энтеробактериями».
4.1. Сбор клинического материала и его упаковку осуществляет
медицинский работник лечебно-профилактического учреждения, обученный
требованиям и правилам биологической безопасности при работе и сборе материала,
подозрительного на зараженность энтерогеморрагическими эшерихиями
(STEC-культуры) E. coli O104:H4. Забор производят в стерильные одноразовые
флаконы, пробирки, контейнеры, стерильными инструментами. Все виды работ
проводят с соблюдением противоэпидемического режима, согласно СП
1.3.2322-08 «Безопасность работы с микроорганизмами III - IV групп
патогенности (опасности) и возбудителями паразитарных болезней».
4.2. Процедуры по забору клинического материала обученный
медицинский персонал осуществляет в резиновых перчатках. После процедуры отбора
материала перчатки обрабатываются растворами дезинфицирующих средств, руки
после снятия перчаток обрабатываются антисептиками в соответствии с СП
1.3.2322-08 «Безопасность работы с микроорганизмами III - IV групп
патогенности (опасности) и возбудителями паразитарных болезней».
От одного больного должно забираться не менее трех видов
клинического материала. Обязательно следует забирать пробы фекалий, промывные
воды из желудка. Каждый образец материала помещают в отдельную транспортную
емкость.
Для постмортальной диагностики используют аутоптаты желудка,
тонкого и толстого кишечника, печени, селезенки, красного костного мозга.
4.3. Сбор материала производят в пробирки с транспортной
средой, предоставляемой (или рекомендуемой) фирмой-производителем тест-систем.
5.1. Все материалы, доставляемые в
лабораторию, должны быть герметично упакованы в соответствии с СП
1.2.036-95 «Порядок учета, хранения, передачи и транспортирования
микроорганизмов I - IV групп патогенности» и настоящих методических указаний:
1) в транспортную емкость (плотно закрывающиеся
пластмассовые пробирки или флаконы с завинчивающимися крышками); плотно
закрытый верхний конец транспортной емкости вместе с крышкой герметизируют
различными пластификаторами (парафин, парафильм и др.); емкость маркируют;
2) в полиэтиленовый пакет подходящего размера с ватой (или
другим гигроскопичным материалом) в количестве достаточном для адсорбции всего
образца в случае его утечки; полиэтиленовый пакет следует герметично заклеить или
запаять;
5.1.1. Образцы от одного пациента могут быть упакованы в
один полиэтиленовый пакет. Не допускается упаковывание образцов материалов от
разных людей в один и тот же пакет.
5.1.2. В полиэтиленовый пакет вкладывают бланк направления с
указанием: наименование направляющего учреждения, ФИО больного, возраст, место
жительства, предварительный диагноз, эпидемиологический анамнез, вид материала,
дата и время взятия материала.
5.2. Герметично закрытые полиэтиленовые пакеты помещают в
термоизолирующий плотно закрывающийся контейнер (термос), приспособленный для
транспортирования биологических материалов.
5.2.1. В термоконтейнеры и термосы помещают охлаждающие
элементы или пакеты со льдом. К наружной стенке термоконтейнера или термоса
прикрепляют этикетку с указанием вида материала, условий транспортирования,
названия пункта назначения.
5.3. Транспортирование проб клинического материала в
референс-лаборатории, лаборатории центров гигиены и эпидемиологии в субъектах
Российской Федерации и лаборатории учреждений противочумной системы
Роспотребнадзора осуществляется нарочным(и), информированным о правилах
доставки материала в соответствии с п. 3.4. СП
1.2.036-95.
6.1. Выделение
и идентификация E. coli О104.Н4 из клинического материала
6.1.1.
Исследование материала
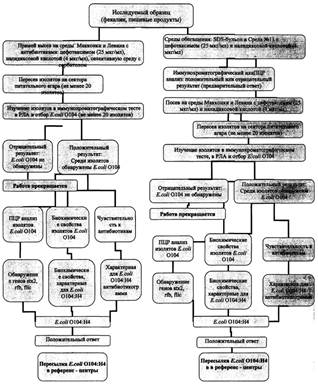
Первый день исследований.
1) Исследуемый материал засевают на
дифференциально-диагностические плотные питательные среды МакКонки и Левина с
антибиотиками: цефотаксимом (25 мкг/мл) и налидиксовой кислотой (4 мкг/мл),
селективный агар с сорбитолом, а также на жидкие питательные среды: питательную
среду для выделения и идентификации энтеробактерий - SDS-бульон,
Мак-Конки-бульон или питательную среду для предварительного обогащения бактерий
семейства Enterobacteriaceae - среду № 11 с теми же антибиотиками: цефотаксимом
(25 мкг/мл) и налидиксовой кислотой (4 мкг/мл).
Посевы инкубируют при 37 °С в течение 18 - 24 часов.
Посевы на плотные среды производят таким образом, чтобы
получить изолированный рост колоний кишечной палочки.
Приготовление указанных выше сред с антибиотиками см. в
Приложении 1.
Второй день исследований.
1) Со сред МакКонки и Левина с антибиотиками
отсевают по 10 типичных для E. coli колоний на отдельные сектора питательного агара
(среда № 1 - ГРМ, СПА или аналог), разлитого в чашки Петри (по 10 изолятов на
одну чашку). Посевы выращивают при 37 °С в течение 18 - 24 часов.
2) Проводят анализ культур выросших на средах МакКонки и
Левина с антибиотиками, на селективном агаре с сорбитолом, с последующим
индукцией синтеза веротоксинов на питательном бульоне, содержащий индуктор
синтеза веротоксинов - карбадокс, с дальнейшим определением веротоксинов с
помощью иммунохроматографических экспресс-тестов для определения
энтерогеморрагических E. coli. Подготовку образца для анализа и постановку
иммунохроматографического теста проводят в соответствии с инструкцией по
применению (см. Приложение 2).
При получении положительных результатов в иммунохроматографическом тесте дают
предварительный ответ на наличие в исследуемом образце энтерогеморрагических
кишечных палочек.
3) Проводят анализ культур, выросших на бульоне с
антибиотиками, с помощью диагностической мультиплексной ПЦР-тест-системы, предназначенной
для индикации клеток штамма E. coli O104:H4 по наличию в генов rfb, stx2 и
flic. Подготовку образца для анализа и постановку ПЦР проводят в соответствии с
Инструкцией по ее применению (см. Приложение 3).
При получении положительных результатов в ПЦР дают
предварительный ответ на наличие в исследуемом образце клеток штамма E. coli
О104:Н4.
4) Проводят высев культур микроорганизмов, выросших на
SDS-бульоне и других бульонах, на чашки Петри со средами МакКонки и Левина,
содержащих цефотаксим (25 мкг/мл) и налидиксовую кислоту (4 мкг/мл),
селективный агар с сорбитолом с таким расчетом, чтобы получить изолированные
колонии E. coli. Посевы выращивают при 37 °С в течение 18 - 24 часов.
Третий день исследований.
1) Проводят анализ культур выросших на
средах МакКонки и Левина с антибиотиками, селективном агаре с сорбитолом, с
последующим индукцией синтеза веротоксинов на питательном бульоне, содержащий индуктор
синтеза веротоксинов - карбадокс и определении веротоксинов с помощью
иммунохроматографических экспресс-тестов для определения энтерогеморрагических
E. coli.. Подготовку образца для анализа и постановку иммунохроматографического
теста проводят в соответствии с инструкцией по применению (см. Приложение 2). При получении положительных
результатов в иммунохроматографическом тесте дают предварительный ответ на
наличие в исследуемом образце энтерогеморрагических кишечных палочек.
2) Используя антительную латексную тест-систему для
индикации эшерихий серогруппы О104, в реакции латексной агглютинации (РЛА)
среди 20 выросших на питательном агаре изолятов проводят поиск культур
серогруппы О104. Постановку РЛА проводят согласно Инструкции по ее применению
(см. Приложение 4). Давшие
положительную реакцию агглютинации с латексным диагностикумом изоляты в этот же
день анализируют с помощью мультиплексной ПЦР-тест-системы согласно инструкции
по ее применению (см. Приложение 3).
Одновременно у культур, которые по результатам РЛА были отнесены к серогруппе
О104, изучают биохимические свойства и определяют у них чувствительность к
антибиотикам (см. Приложение 5).
3) Проводят пересев 20 типичных для E. coli изолятов,
выросших на средах МакКонки и Левина с антибиотиками, селективном агаре с
сорбитолом (после пересева культур со сред обогащения - SDS-бульона и др.) на
отдельные сектора чашек Петри с питательным агаром (по 10 изолятов на чашку).
Четвертый день исследований.
1) В случае, если при положительном иммунохроматографическом
тесте, ПЦР-анализе в культурах изолятов, полученных прямым высевом из образца
(см. Второй день исследований, п. 1.) и
давших положительную реакцию агглютинации с латексным диагностикумом (см.
Третий день исследований, п. 1.) и, были
обнаружены культуры, продуцирующие веротоксин, или были идентифицированы гены
rfb, stx2 и flic, специфичные для эпидемического штамма E. coli О104:H4, и
культуры по своим биохимическим свойствам соответствуют виду E. coli, то делают
заключение об обнаружении эпидемического штамма E. coli O104:H4 в анализируемом
образце. В этом случае все дальнейшие исследования образца прекращают, а
изолированные культуры E. coli O104:H4 пересылают для дальнейшего их изучения в
референс-центры по мониторингу за возбудителями инфекционных болезней ФГУН ГНЦ
ПМБ Роспотребнадзора, референс-центр по мониторингу за возбудителями острых
кишечных инфекций (ФГУН «Центральный научно-исследовательский институт
эпидемиологии» Роспотребнадзора) и референс-центр по мониторингу за
возбудителями природно-очаговых инфекционных болезней ФГУЗ «Иркутский
научно-исследовательский противочумный институт Сибири и Дальнего Востока»
Роспотребнадзора) (далее референс-центры) с учётом оптимальной транспортной
схемы.
В том случае, если ни один из 20 изолятов, полученных при
прямом высеве анализируемого материала на среды МакКонки и Левина с
антибиотиками, на селективный агар с сорбитолом не дали положительную реакцию
на наличие энтеротоксинов, определяемых в экспрессном иммунохроматографическом
тесте, не дали положительную реакцию в РЛА и ПЦР-исследовании, работу с этими
изолятами прекращают, а их культуры уничтожают.
2) Продолжают работать с 20 изолятами, полученными со сред
обогащения (см. Третий день исследований, п. 1.).
У изолятов определяют наличие веротоксинов после инкубации на питательном
бульоне, содержащий индуктор синтеза веротоксинов - карбадокс (и далее
тестируют с помощью иммунохроматографических экспресс-тестов, изучают серологические
свойства в РЛА, предназначенной для идентификации серогруппы E. coli О104.
В случае обнаружения изолятов, давших положительную реакцию
на наличие веротоксинов в иммунохроматографическом тесте, положительную реакцию
агглютинации в РЛА, их анализируют в ПЦР для обнаружения в геноме исследуемых
изолятов специфических для E. coli О104:Н4 генов rfb, stx2 и flic. У этих же
изолятов изучают биохимические свойства и чувствительность к антибиотикам.
Пятый день исследований.
1) В случае, если при ПЦР-анализе в культурах изолятов,
давших положительную реакцию агглютинации с латексным диагностикумом, были
идентифицированы гены rfb, stx2 и flic, специфичные для штамма E. coli O104:H4,
а культуры по своим биохимическим свойствам соответствуют виду E. coli, то делают
заключение об обнаружении эпидемического штамма E. coli O104:H4 в анализируемом
образце.
В этом случае все дальнейшие исследования образца
прекращают, образец уничтожают, а изолированные культуры E. coli O104:H4
пересылают для дальнейшего их изучения в референс-центры.
В том случае, если ни одна из 20 культур, полученных со сред
обогащения, не была отнесена к серогруппе О104, работу с этими изолятами
прекращают, а их культуры уничтожают.
Делается заключение об отсутствии в исследуемом материале
эпидемического штамма Е. coli О104:Н4.
6.2.1.
Взятие материала и пересылка его для лабораторного исследования
При отборе и подготовке образцов различных видов пищевых
продуктов к исследованию руководствуются МУК 4.2.2812-11, Москва, 2011, «Методы
выявления и идентификации патогенных бактерий - возбудителей инфекционных
заболеваний с пищевым путем передачи в продуктах питания на основе ПЦР с
гибридизационно-флуоресцентной детекцией».
6.2.2.
Исследование материала
Выделение культур E. coli O104:H4 из исследуемых образцов
пищевых продуктов и их последующую идентификацию с помощью
иммунохроматографических экспресс-тестов на веротоксины, реакции латексной
агглютинации (РЛА) и мультиплексной ПЦР, определение биохимических свойств и
чувствительности культур к антибиотикам проводят по той же схеме, как и в
случае исследования клинических образцов (см. п. 6.1.).
7.1.1.
Исследование материала
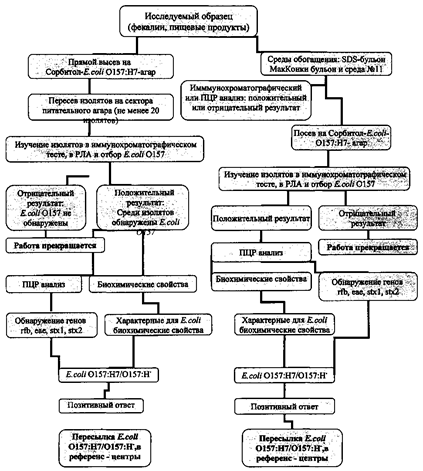
Первый день исследований.
1) Исследуемый материал засевают на среду для выделения и
дифференциации E. coli O157:Н7/О157:Н - Сорбитол-E. coli О157:Н7-агар или
Мак-Конки сорбитол агар и параллельно на обычный агар Эндо или МакКонки агар, а
также на жидкие питательные среды - SDS-бульон и др.
Прямой высев анализируемого образца на Сорбитол E. coli
О157:Н7-агар или идентичные среды необходимо производить не менее чем на три
чашки Петри с таким расчетом, чтобы на пластинках среды вырастали десятки,
сотни изолированных колоний микроорганизмов. Получение большого количества
колоний на дифференциальной среде повышает вероятность обнаружения и выделения
серовара E. coli O157:Н7/О157:Н.
Посевы инкубируют при 37 °С в течение 18 - 24 часов.
Второй день исследований.
1) Среди выросших колоний на Сорбитол - E. coli
О157:Н7-агаре отбирают неокрашенные сорбитолнегативные колонии, характерные для
E. coli О157:Н7, и засевают их на отдельные сектора в чашки Петри с питательным
агаром. При наличии большого количества неокрашенных колоний необходимо отсеять
не менее 20 изолятов (по 10 на чашку). Посевы выращивают при 37 °С в течение 18
- 24 часов.
2) С помощью иммунохроматографических экспресс-тестов
определения E. coli O157:Н7/О157:Н или иммунохроматографических экспресс-тестов
для определения энтерогеморрагических E. coli проводят анализ культур, выросших
на твёрдых питательных средах. Подготовку образца для анализа и постановку
иммунохроматографических экспресс тестов проводят в соответствии с инструкцией
по их применению (см. Приложение 6).
3) С помощью мультиплексной ПЦР (набор «ТЭК-О157» или
аналоги), предназначенной для индикации клеток E. coli O157:Н7/О157:Н по
наличию в них генов rfb, eae, stx1, stx2 (или только stx1 или stx2), проводят
анализ смеси культур, выросших на SDS-бульоне или других жидких средах.
Подготовку образца для анализа и постановку ПЦР проводят в соответствии с
Инструкцией по ее применению (см. Приложение 7).
При получении положительных результатов
иммунохроматографических экспресс-тестов или в ПЦР-исследовании дают
предварительный ответ на наличие в исследуемом образце клеток
энтерогеморрагического серовара E. coli O157:Н7/О157:Н.
3) Проводят пересев культур микроорганизмов, выросших на
жидких средах, на чашки Петри со средой Сорбитол-E. coli О157:Н7-агар, (по три
чашки из каждой среды) с таким расчетом, чтобы получить десятки и сотни
изолированные колонии микроорганизмов. Посевы выращивают при 37 °С в течение 18
- 24 часов.
Третий день исследований.
1) Используя иммунохроматографические экспресс-тесты
определения E. coli O157:Н7/О157:Н, антительную латексную тест-систему для
индикации E. coli серогруппы О157, в реакции латексной агглютинации (РЛА) среди
выросших на питательном агаре изолятов, полученных из неокрашенных
сорбитолнегативных колоний (взятых после прямого посева образца с Сорбитол-E.
coli О157:Н7-агара, проводят поиск культур E. coli серогруппы О157. Постановку
РЛА проводят согласно Инструкции по ее применению (см. Приложение 8). Давшие положительную реакцию
в иммунохроматографических экспресс-тестах определения E. coli O157:Н7/О157:Н
или реакции агглютинации с латексным диагностикумом культуры в этот же день
анализируют с помощью мультиплексной ПЦР-тест-системы. Одновременно у культур,
которые по результатам РЛА были отнесены к серогруппе О157, изучают
биохимические свойства.
2) Производят пересев сорбитолнегативных
неокрашенных колоний, выросших на Сорбитол-E. coli О157:Н7-агаре или идентичных
средах (после пересева культур со сред обогащения), на отдельные сектора
пластинок питательного агара, разлитого в чашки Петри. При наличии на
Сорбитол-E. coli О157:Н7-агаре большого количества сорбитолнегативных колоний
необходимо отсеять для последующих исследований не менее 20 изолятов (по 10
колоний на чашку).
Четвертый день исследований.
1) В случае, если при ПЦР-анализе в культурах изолятов,
выделенных прямым высевом анализируемого образца на Сорбитол-E. coli
О157:Н7-агар и давших положительную реакцию в иммунохроматографических
экспресс-тестах для определения E. coli O157:Н7/О157:Н или агглютинации с
латексным диагностикумом, были идентифицированы гены rfb, eae, stx1 и stx2 (или
только stx1 или stx2), специфичные для серовара E. coli O157:Н7/О157:Н, и
культуры по своим биохимическим свойствам соответствуют виду E. coli, то делают
заключение об обнаружении в анализируемом материале клеток
энтерогеморрагического серовара E. coli O157:Н7/О157:Н. В этом случае все
дальнейшие исследования образца прекращают, а изолированные культуры E. coli
O157:Н7/О157:Н пересылают для дальнейшего их изучения в референс-центры.
В том случае, если ни один из изолятов, полученных при
прямом высеве анализируемого материала на Сорбитол-E. coli О157:Н7-агар, не дал
положительную реакцию в иммунохроматографических экспресс-определения E. coli
O157:Н7/О157:Н или РЛА, работу с этими изолятами прекращают, а их культуры
уничтожают.
2) У сорбитолнегативных изолятов, полученных со сред
обогащения (см. Третий день исследований, п. 2.),
определяют принадлежность к E. coli O157:Н7/О157:Н на иммунохроматографических
экспресс-тестах, изучают серологические свойства в РЛА, предназначенной для идентификации
E. coli серогруппы О157.
В случае обнаружения изолятов, давших положительную реакцию
на иммунохроматографических экспресс-тестах, положительную реакцию агглютинации
в РЛА, их анализируют в ПЦР для обнаружения в их геноме специфических для E. coli
O157:Н7/О157:Н генов rfb, eae, stx1 и stx2 (или только stx1 или stx2). У этих
же изолятов изучают биохимические свойства.
Пятый день исследований.
1) В случае, если при ПЦР-анализе в культурах изолятов,
давших положительную реакцию на иммунохроматографических экспресс-тестах,
положительную реакцию агглютинации с латексным диагностикумом, были
идентифицированы гены rfb, eae, stx1, stx2 (или только stx1 или stx2),
специфичные для E. coli O157:Н7/О157:Н, и культуры по своим биохимическим
свойствам соответствуют виду E. coli, то делают заключение об обнаружении
штамма E. coli O157:Н7/О157:Н в анализируемом образце.
В этом случае все дальнейшие исследования образца
прекращают, образец уничтожают, а изолированные культуры E. coli O157:Н7/О157:Н
пересылают для дальнейшего их изучения в референс-центры.
В том случае, если ни один из изолятов, полученных со сред
обогащения, не был отнесен к серогруппе О157, работу с этими изолятами
прекращают, а их культуры уничтожают.
Делается заключение об отсутствии в исследуемом материале
бактерий энтерогеморрагического серовара E. coli O157:Н7/О157:Н.
7.2.1.
Взятие материала и подготовка его для лабораторного исследования
При отборе и подготовке образцов различных видов пищевых
продуктов к исследованию руководствуются МУК 4.2.2812-11, Москва, 2011, «Методы
выявления и идентификации патогенных бактерий - возбудителей инфекционных
заболеваний с пищевым путем передачи в продуктах питания на основе ПЦР с гибридизационно-флуоресцентной
детекцией», МУК
4.2.992-00 «Методы выделения и идентификации энтерогеморрагической кишечной
палочки E. coli О157:Н7» и МУ № 04-723/3 от 17.12.84 г. «По микробиологической
диагностике заболеваний, вызываемых энтеробактериями».
7.2.2.
Исследование материала
Выделение культур E. coli O157:Н7/О157:Н из исследуемых
образцов и их последующую идентификацию с помощью иммунохроматографических
экспресс-тестов, реакции латексной агглютинации (РЛА) (для обнаружения
серогруппы О157) и мультиплексной ПЦР-тест-системы, определение биохимических
свойств культур проводят по той же схеме, как и в случае исследования
клинических образцов (см. п. 5.1.).
8.1.1.
Исследование материала
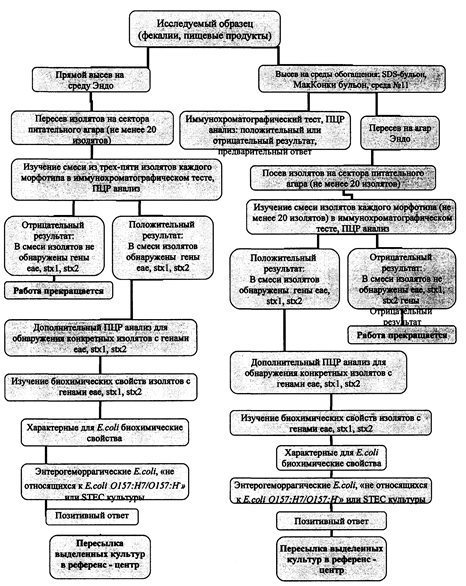
Первый день исследований.
1) Исследуемый материал засевают на три чашки Петри с питательной
средой для выделения энтеробактерий - агар Эндо, селективный агар Мак Конки с
сорбитолом и на среды для предварительного обогащения энтеробактерий -
SDS-бульон, МакКонки-бульон или среду № 11.
Высев материала на дифференциально-диагностические плотные
среды производят с таким расчетом, чтобы в каждой чашке или в сумме на трех
чашках получить не менее 100 изолированных колоний энтеробактерий.
Посевы выращивают при 37 °С в течение 18 - 24 часов.
Второй день исследований.
1) Просматривают результаты посевов на
дифференциально-диагностических средах и оценивают морфологию выросших
изолированных колоний энтеробактерий (определяют морфотип колоний). Затем на
чашки Петри с питательным агаром засевают по три - пять колоний каждого
морфотипа (на отдельные сектора среды). Число отсеянных изолятов при любом
количестве морфотипов не должно быть менее 20. Посевы выращивают при 37 °С в
течение 18 - 24 часов.
2) Проводят анализ культур выросших на средах МакКонки и
Левина с антибиотиками, селективном агаре МакКонки с сорбитолом, с помощью
иммунохроматографических экспресс-тестов для определения энтерогеморрагических
E. coli. Подготовку образца для анализа и постановку иммунохроматографического
теста проводят в соответствии с инструкцией по применению (см. Приложение 2).
3) Используя мультиплексную
ПЦР-тест-систему, проводят анализ смеси культур энтеробактерий, выросших на
жидких накопительных средах (SDS-бульон, среда № 11), на присутствие в них
энтерогеморрагических эшерихий, «не относящихся к E. coli О157:H7».
Идентифицируют такие эшерихии на основании обнаружения в смеси энтеробактерий
генов еае, stx1, stx2 (или только stx1 или stx2). Ген rfb, определяющий синтез
антигена О157, в этой группе патогенов не обнаруживается. Следует также
учитывать, что в отдельных случаях у энтерогеморрагических культур, «не
относящихся к E. coli О157:H7», может не обнаруживаться и ген еае.
При получении положительных результатов
иммунохроматографических экспресс-тестов для определения энтерогеморрагических
E. coli, в ПЦР (обнаружение генов еае, stx1, stx2) дают предварительный ответ
на наличие в исследуемом образце клеток энтерогеморрагических эшерихий, «не
относящихся к E. coli О157:H7».
3) Производят высев культур энтеробактерий, выросших на
жидких накопительных средах (SDS-бульон, среда № 11 или аналоги), на чашки
Петри со средой Эндо, МакКонки-агаром с сорбитолом (не менее чем на три чашки с
каждой среды обогащения) с таким расчетом, чтобы получить не менее 100
изолированные колонии микроорганизмов. Посевы выращивают при 37 °С в течение 18
- 24 часов.
Третий день исследований.
1) С помощью ПЦР-исследований проводят
анализ 3 - 5 смешанных в одной пробирке изолятов энтеробактерий каждого
морфотипа, отобранного при прямом высеве исследуемого материала (см. Второй
день исследований, п. 1). Для получения
более объективных результатов анализа, при любом количестве отобранных
морфотипов, число изучаемых в ПЦР изолятов должно быть не менее 20.
Результатами ПЦР анализа смеси изолятов могут быть:
а) в смеси изолятов обнаруживают гены еае, stx1, stx2;
б) в смеси изолятов обнаруживают еае-ген и один из
stx-генов;
в) в смеси изолятов обнаруживают только stx1- и stx2-гены
(или один из них) и не обнаруживают ген еае.
При обнаружении в смеси изолятов одной из перечисленных выше
комбинаций генов проводят дополнительную ПЦР с каждым из входящих в смесь
трех-пяти изолятов. У каждого изолята, давшего положительную ПЦР, определяют
биохимические свойства для подтверждения принадлежности его к виду Е. coli.
2) Просматривают результаты посевов со сред
накопления на среду Эндо (см. Второй день исследований п. 3) и оценивают морфологию изолированных колоний
энтеробактерий. Затем по три - пять колоний бактерий каждого морфотипа засевают
на отдельные сектора питательного агара в чашках Петри. Число отсеянных
изолятов, независимо от количества выявленных среди колоний морфотипов, должно
составлять не менее 20. Посевы выращивают при 37 °С в течение 18 - 24 часов.
3) Проводят анализ культур выросших на средах МакКонки и
Левина с антибиотиками, с помощью иммунохроматографических экспресс-тестов для
определения энтерогеморрагических E. coli. Подготовку образца для анализа и
постановку иммунохроматографического теста проводят в соответствии с
инструкцией по применению (см. Приложение 2).
Четвертый день исследований.
1) Учитывают результаты изучения
биохимических свойств изолятов, в которых с помощью ПЦР были обнаружены
специфические для энтерогеморрагических эшерихий гены еае, stx1, stx2 (или
только один из генов шигатоксинов) (см. Третий день исследований, п. 1). В случае, если изолят по своим биохимическим
свойствам соответствует виду E. coli, делают заключение о присутствии в
анализируемом образце энтерогеморрагических эшерихий, «не относящихся к E. coli
О157:H7».
В том случае, если изолят по своим биохимическим свойствам
соответствует виду E. coli, определяется положительный результат в
иммунохроматографическом экспресс-тесте для определения энтерогеморрагических
E. coli, но у культуре не обнаружен ген еае, а присутствуют лишь гены
шига-токсинов, делают заключение о присутствии в анализируемом образце
шига-токсинпродуцирующих эшерихий (STEC-культур).
При обнаружении в образце энтерогеморрагических изолятов
эшерихий или STEC-изолятов, исследования прекращают, а выделенные культуры
направляют в референс-центры для дальнейшего изучения.
Если у изученных штаммов с помощью ПЦР-исследований
обнаружены гены еае, stx1, stx2 или же эти гены в разной комбинации, но изоляты
по своим биохимическим свойствам не могут быть отнесены к виду E. coli, делают
заключение об отсутствии в исследуемом образце энтерогеморрагических или
STEC-культур. Выделенные культуры с генами еае, stx1, stx2, но не относящиеся к
виду E. coli, также направляют в референс-центры.
2) Если в четвертый день исследований по п. 1 получены отрицательные результаты, продолжают поиск
энтерогеморрагических эшерихий или STEC-культур среди изолятов энтеробактерий,
выделенных из сред обогащения (см. Третий день исследований, п. 2).
Изучение изолятов в ПЦР проводят по той же схеме, как это
описано выше (см. Четвертый день исследований, п. 1). Если в результате проведенного анализа идентифицированы
культуры энтеробактерий с генами еае, stx1, stx2, изучают их биохимические
свойства.
Пятый день исследований.
1) Учитывают результаты изучения биохимических свойств
изолятов энтеробактерий с генами еае, stx1, stx2. В случае, если эти изоляты по
биохимическим свойствам относятся к виду E. coli, то делают положительное
заключение о наличии в исследуемом образце энтерогеморрагических эшерихий или
STEC-культур.
Выделенные культуры направляют в референс-центры.
8.2.1.
Исследование материала
Выделение энтерогеморрагических культур E. coli «не
относящихся к E. coli О157:H7» из исследуемых образцов и их последующую
идентификацию в иммунохроматографических экспресс-тестах, с помощью
мультиплексной ПЦР и определения биохимических свойств культур проводят по той
же схеме, как и в случае исследования клинических образцов (см. п. 6.1.).
В соответствии с утвержденными санитарно-эпидемиологическими
правилами СП 1.3.2885-11 «Дополнения и изменения № 2 к СП
1.3.2322-08 «Безопасность работы с микроорганизмами III - IV групп патогенности
(опасности) и возбудителями паразитарных болезней», утвержденными
постановлением Главного государственного санитарного врача Российской Федерации
от 29.06.2011 № 86 (зарегистрированы в Минюсте России 30.06.2011,
регистрационный номер 63953), дополнено приложение 1 «Классификация микроорганизмов - возбудителей
инфекционных заболеваний человека, простейших, гельминтов и ядов биологического
происхождения по группам патогенности» раздел «Бактерии», подраздел «II группа»
следующим пунктом: Escherichia coli О157:Н7, О104:Н4 и другие серотипы -
продуценты веротоксина (возбудители геморрагического колита,
гемолитико-уремического синдрома). Таким образом, возбудители E. coli O104:H4 и
О157:Н7 относятся к II группе патогенности, и для работы с ними требуется
наличие у лаборатории соответствующего санитарно-эпидемиологического
заключения.
Все работы по сбору, транспортированию и подготовке проб
клинического и секционного материала осуществляют в соответствии с требованиями
СП
1.3.2322-08 «Безопасность работы с микроорганизмами III - IV групп
патогенности (опасности) и возбудителями паразитарных болезней», СП 1.3.2518-09
«Безопасность работы с микроорганизмами III - IV групп патогенности (опасности)
и возбудителями паразитарных болезней. Дополнения и изменения 1 к СП
1.3.2322-08», СП
1.2.036-95 «Порядок учета, хранения, передачи и транспортирования
микроорганизмов I - IV групп патогенности», методических указаний МУ
1.3.2569-09 «Организация работы лабораторий, использующих методы
амплификации нуклеиновых кислот при работе с материалом, содержащим
микроорганизмы I - IV групп патогенности».
Лабораторные исследования на энтерогеморрагические кишечные
палочки, в том числе E. coli О104:Н4 и О157:Н7, проводят бактериологические
лаборатории юридических лиц, независимо от организационно-правовых форм и форм
собственности, в том числе центров гигиены и эпидемиологии,
лечебно-профилактических, ведомственных и противочумных учреждений, имеющих
санитарно-эпидемиологические заключения и лицензии на право работы с
микроорганизмами II - IV и III - IV групп патогенности.
3.1. Показания к проведению исследований.
Исследования клинического материала проводятся в случае:
- Наличия у пациента гемолитико-уремического синдрома после
(на фоне) перенесенного диарейного заболевания.
- Наличия у пациента гемолитической анемии после (на фоне)
перенесенного диарейного заболевания.
- Наличия у пациента любого (по тяжести и синдромальному
диагнозу) диарейного заболевания при наличии эпидемиологических данных о
возможной связи заболевания с ЕНЕС.
Исследования образцов продуктов питания проводятся по
эпидемиологическим показаниям в соответствии с действующими
нормативно-методическими документами.
Бактериологические лаборатории учреждений
лечебно-профилактических и ведомственных служб, центров гигиены и
эпидемиологии, имеющих санитарно-эпидемиологические заключения и лицензии на
право работы с микроорганизмами III - IV групп патогенности:
Проводят плановые диагностические исследования материала от
больных острыми кишечными инфекциями, определенного контингента здоровых лиц и
проб из объектов окружающей среды.
Забор материала от пациентов (или умерших) с подозрением на
инфекционное заболевание, вызванное STEC-культурами, проводят в
лечебно-профилактических учреждениях (ЛПУ), в максимально ранние сроки до
назначения антибактериальной терапии. В качестве клинического материала для
исследований используют образцы фекалий. Для постмортальной диагностики
используют содержимое кишечника, аутоптаты желудка, тонкого и толстого
кишечника, почек. Сбор материала производят в пробирки с транспортной средой,
предоставляемой (или рекомендуемой) фирмой-производителем тест-систем.
Исследования ведут до установления отрицательного результата
анализа или выделения культур микроорганизмов, подозрительных на
энтерогеморрагические кишечные палочки (положительные результаты при
использовании иммунохроматографических экспресс-тестов для определения
энтерогеморрагических E. coli, реакцией РЛА или ПЦР на E. coli O104:H4 и
О157:Н7.
При подозрении на положительный результат выделения культур
энтерогеморрагических кишечных палочек сотрудники лабораторий немедленно
сообщают в Управление Роспотребнадзора в субъекте Российской Федерации. Для
окончательной идентификации выделенные культуры по согласованию с Управлением
Роспотребнадзора в субъекте Российской Федерации направляют в установленном
порядке в лаборатории особо опасных инфекций центров гигиены и эпидемиологии в
субъектах Российской Федерации, имеющих санитарно-эпидемиологические заключения
и лицензии на право работы с микроорганизмами II - IV групп патогенности.
Доставка материала производится транспортом
лечебно-профилактических учреждений по согласованию с управлением
Роспотребнадзора субъекта Российской Федерации с учётом оптимальной
транспортной схемы.
Лаборатории особо опасных инфекций центров гигиены и
эпидемиологии в субъектах Российской Федерации, имеющих
санитарно-эпидемиологические заключения и лицензии на право работы с
микроорганизмами II - IV групп патогенности:
- выполняют исследование материала от больных и умерших с
подозрением на эшерихиозную инфекцию и объектов окружающей среды с целью
индикации возбудителя;
- идентифицируют культуры, выделенные в лабораториях,
определяя их таксономическую принадлежность, и эпидемическую значимость
(токсигенность), а также чувствительность к антибиотикам;
- осуществляют (или организуют) бактериологический контроль
качества питательных сред и других диагностических препаратов, используемых в
лабораториях;
- представляют оперативную информацию о выделенных культурах
в Управление Роспотребнадзора в субъекте Российской Федерации;
- контролируют деятельность территориальных лабораторий,
оказывают им методическую помощь по всем вопросам лабораторного обеспечения
эпидемиологического надзора.
При необходимости проведения оценки идентичности изолятов -
направляют культуры ЕНЕС в референс-центры по мониторингу за возбудителями
инфекционных болезней ФГУН ГНЦ ПМБ Роспотребнадзора, референс-центр по
мониторингу за возбудителями острых кишечных инфекций (ФГУН «Центральный научно-исследовательский
институт эпидемиологии» Роспотребнадзора) и референс-центр по мониторингу за
возбудителями природно-очаговых инфекционных болезней ФГУЗ «Иркутский
научно-исследовательский противочумный институт Сибири и Дальнего Востока»
Роспотребнадзора) с учётом оптимальной транспортной схемы.
Референс-центры:
- проводят исследования материала или культур от больных и
умерших с подозрением на заболевание эшерихиозом, а также объектов окружающей
среды;
- подтверждают таксономическую принадлежность культур,
выделенных на курируемой территории;
- проводят субвидовое типирование выделенных изолятов
STEC-культур в соответствии с поставленными эпидемиологическими задачами с
применением унифицированных протоколов анализа набора продуктов рестрикции
тотальной ДНК в пульсирующем электрическом поле - пульс-электрофорез (PFGE -
Pulsed Field Gel Electrophoresis).
- идентифицируют все атипичные культуры с использованием
дополнительных методов серологической, биохимической и других видов
идентификации с целью уточнения таксономической принадлежности;
- определяют эпидемическую значимость (токсигенность)
культур, с использованием комплекса регламентированных методов,
антибиотикочувствительность;
- осуществляют методическое руководство по всем вопросам
лабораторного обеспечения эпидемиологического надзора на курируемой территории;
- в установленном порядке передают с паспортами выделенные
культуры в Государственную коллекцию патогенных бактерий ФБУН ГНЦ ПМБ.
Референс-центр по мониторингу за возбудителями острых кишечных
инфекций (ФГУН «Центральный научно-исследовательский институт эпидемиологии»
Роспотребнадзора) осуществляет ведение единой общероссийской базы данных по
циркулирующим в Российской Федерации штаммам STEC-культур и их депонирование в
Национальном центре верификации диагностической деятельности на базе ФГУН ГНЦ
ПМБ Роспотребнадзора.
Результаты исследований, проводимых на каждом уровне,
передают в Федеральную службу по надзору в сфере защиты прав потребителей и
благополучия человека, в управление Роспотребнадзора по субъекту Российской
Федерации, в учреждение, направившее материал, в день получения результата.
Персонал лабораторий, выполняющих исследования на
эшерихиозы, должен быть подготовлен по вопросам лабораторной диагностики,
техники безопасности и обеспечен соответствующими инструктивно-методическими
материалами.
Усовершенствование врачей-бактериологов и лаборантов по
микробиологии и лабораторной диагностике эшерихиозов проводят на специальных
курсах усовершенствования.
Приложение 1
Приготовление питательных сред с антибиотиками для
селективного выделения изолятов E. coli О104:Н4 из клинического материала и
пищевых продуктов
В качестве селективных питательных сред для выделения
Escherichia coli О104:Н4 из исследуемого материала используют: плотные дифференциально-диагностические
среды МакКонки и Левина и жидкие накопительные среды SDS-бульон, TSB-бульон и
среду № 11 ГРМ, в которые добавлены антибиотики цефотаксим (25 мкг/мл) и
налидиксовая кислота (4 мкг/мл).
Указанные выше среды готовят согласно прописи производителя:
- агар МакКонки-ГРМ - 25 г порошка растворить в 500 мл
дистиллированной воды, кипятить в течение 3 мин и стерилизовать
автоклавированием при 121 °С (1 атм.) в течение 15 мин.
- агар Левина-ГРМ - 17 г порошка растворить в 500 мл
дистиллированной воды, кипятить в течение 2 - 3 мин, профильтровать через
ватно-марлевый фильтр и стерилизовать автоклавированием при 110 °С (0,5 атм.) в
течение 20 мин.
- SDS-бульон - 3.2 г порошка растворить в 100 мл
дистиллированной воды Прокипятить 1 - 2 мин. Не автоклавировать.
- Среда № 11 ГРМ - 27,08 г препарата размешивают в 1 л
дистиллированной воды, кипятят в течение 2 мин, фильтруют через ватно-марлевый
фильтр и стерилизуют автоклавированием при температуре 121 °С в течение 15
минут.
Приготовленные среды охладить до температуры 40 - 45 °С и
внести в них растворы антибиотиков до конечной концентрации: цефотаксима - 25
мкг/мл, налидиксовой кислоты - 4 мкг/мл. Разлить агар по чашкам, а бульон - в
колбы в количестве 100 мл.
Приготовление антибиотиков:
- Цефотаксим (ОАО «Биосинтез», Россия или аналог).
Антибиотик взвешивают на аналитических или торсионных весах
в количестве 100 мг и растворяют навеску в 10 мл дистиллированной воды.
Получают концентрацию препарата 10 мг/мл
- вносят антибиотик в объеме 0,25 мл на 100 мл среды
(конечная концентрация 25 мкг/мл) или
- 1,25 мл на 500 мл среды (конечная концентрация 25 мкг/мл)
- Налидиксовая кислота («Неграм» KRKA, Словения, или
аналог).
На аналитических или торсионных весах взвешивают 16 мг
антибактериального препарата и растворяют его в 5 мл дистиллированной воды, в
которую по каплям при постоянном перемешивании вносят I№ раствор NaOH до полного растворения препарата и доводят общий объем
дистиллированной водой до 10 мл. Получают концентрацию препарата 1,6 мг/мл
- вносят антибактериальный препарат в объеме 0,25 мл на 100
мл среды (конечная концентрация 4 мкг/мл) или
- 1,25 мл на 500 мл среды (конечная концентрация 4 мкг/мл)
На указанных выше средах с антибиотиками хорошо вырастает
культура E. coli О104:Н4, но подавляется рост энтеробактерий, чувствительных к
цефотаксиму и налидиксовой кислоте.
Приложение 2
Инструкция
по применению экспресс-теста для определения энтерогеморрагических E. coli
Иммунохроматографический экспресс-тест, который выявляет наличие
веротоксинов (шигоподных токсинов), продуцируемых энтерогеморрагическими (ЕНЕС)
патогенными штаммами E. coli (включая E. coli О157:H7), при выделении из
пищевых продуктов.
Принцип работы иммунохроматографического теста основан на
взаимодействии антигенов, находящихся в образце исследуемого материала с
антителами, меченными золотом. Иммунохроматографический тест (Duopath ®
Verotoxins или аналоги) представляет собой диагностическую тест-панель с
круглой лункой для добавления образца, овальным окном с тестовыми зонами (VT1)
и (VT2) и контрольной (С) зоной.
1) Образец добавляется в круглую лунку.
2) Образец адсорбируется подложкой и взаимодействует со
специфичными к веротоксинам (VT1) и (VT2) антителами.
3) В присутствии антигенов (веротоксинов) образуется
комплекс с меченными антителами, который мигрирует до зоны связывания в
тестовой зоне (VT1) и (VT2).
4) Зоны связывания (VT1) и (VT2) содержат соответствующие
антитела к комплексу антиген-антитело. В результате образуется четкая красная
линия в одной зоне (VT1) (наличие веротоксинов группы 1) или в другой зоне
(VT2) (наличие веротоксинов группы 2) или в двух зонах сразу при наличии
веротоксинов обеих групп (VT1) и (VT2).
5) Оставшийся образец продолжает движение к контрольной зоне
(С) и образует четкую красную линию, указывающую на то, что тест работает
правильно.
Чувствительность метода - нижний предел обнаружения
веротоксинов составляет 25 нг/мл для веротоксинов группы 1 (VT1) и 62,5 нг/мл
для веротоксинов группы 2 (VT2).
Условия хранения
Иммунохроматографические тесты стабильны до даты, указанной
на упаковке, при хранении в условиях +2 - 8 °С.
Проведение
анализа
(I)
Выявление энтерогеморрагических E. coli в образцах пищевых продуктов
1) Смешать 25 г (мл) образца с 225 мл среды обогащения.
Выбор среды обогащения зависит от типа продукта. Среда для молочных продуктов -
модифицированный триптиказо-соевый бульон с новобиоцином. Среда для мясных
продуктов - модифицированный бульон ЕС с новобиоцином.
2) При необходимости гомогенизировать образец. Инкубировать
триптиказо-соевый бульон с новобиоцином в течение 18 - 24 ч при 37 °С, а
модифицированный бульон ЕС с новобиоцином в течение 18 - 24 ч при 41,5 °С.
3) Со среды обогащения посеять на Макконки агар с сорбитолом
и инкубировать в течение 18 - 24 ч при 37 °С.
4) Выбрать 1 - 5 характерные колонии E. coli со Макконки
агара с сорбитолом.
5) Ресуспендировать колонии в 1 мл бульона с добавкой
индуктора синтеза веротоксинов.
6) Инкубировать в течение 6 часов при 37 °С.
7) Перенести 180 мкл культуральной жидкости бульона с
добавлением индукторов синтеза веротоксинов в пластиковую пробирку (эппендорф).
8) К флакону с полимиксином В добавить 1 мл стерильной
дистиллированной воды.
9) Добавить 20 мкл раствора полимиксина В к 180 мкл
культуральной жидкости с бульоном с добавкой индуктора синтеза веротоксинов и
перемешать. Инкубировать в течение 10 минут при 37 °С.
10) Дать остыть до комнатной температуры.
Примечание. На агаре Мак-Конки с сорбитолом и селективной
добавкой СТ способны расти только штаммы E. coli О157. Для определения синтеза
веротоксинов от других сероваров E. coli, должен быть заменен на Макконки агар
с сорбитолом или агар с сердечно-мозговой вытяжкой.
Проведение
тестирования
1) Перед использованием обогащенный образец и
иммунохроматографический тест должны быть комнатной температуры (обычно тесты
хранятся в холодильнике).
2) Вскрыть пакет из фольги, в который упакован тест.
3) Положить тест на ровную поверхность и отмаркировать
(указать номер исследуемого образца). Тестирование должно быть проведено в
течение 2 часов после вскрытия фольги!
4) Используя микропипетку и одноразовый наконечник, добавить
150 мкл охлажденной культуральной жидкости в круглую лунку для образца.
5) Считать результаты через 20 минут после добавления
образца.
Интерпретация
результатов
1) Результаты теста учитываются только при наличии четкой
красной линии в контрольной зоне (С) через 20 минут.
2) Образец считается положительным, если после 20 минут или
ранее красные линии образовались как в тестовых зонах (VT1) и/или (VT2), так и
в контрольной (С) зоне.
3) Образец считается отрицательным, если красная линия
отсутствует в тестовых зонах (VT1) и/или (VT2), но присутствует в контрольной
зоне (С).
4) Тест следует повторить, если красные линии отсутствуют
как в тестовых зонах (VT1) и/или (VT2), так и в контрольной зоне (С) через 20
минут.
(II)
Выявление энтерогеморрагических E. coli из клинического материала
1) Посеять клинический материал (фекалии) на агар Мак Конки
с сорбитолом и инкубировать 18 - 24 часа при 37 °С.
2) Снять тампоном выросшие на агаре колонии, пересекая
несколько раз зону сливного роста.
3) Ресуспендировать колонии в 1 мл бульона с добавкой
индуктора синтеза веротоксинов. Инкубировать в течение 6 часов при 37 °С.
4) Перенести 180 мкл культуральной жидкости бульона с
добавкой индуктора синтеза веротоксинов в пластиковую пробирку (эппендорф).
5) К флакону с полимиксином В добавить 1 мл стерильной
дистиллированной воды. Добавить 20 мкл раствора полимиксина В к 180 мкл
культуральной жидкости с CAYE-бульоном и перемешать. Инкубировать в течение 10
минут при 37 °С.
6) Дать остыть до комнатной температуры.
Проведение
тестирования
1) Перед использованием обогащенный образец и
иммунохроматографический тест должны быть комнатной температуры (обычно тесты
хранятся в холодильнике).
2) Вскрыть пакет из фольги, в который упакован тест.
3) Положить тест на ровную поверхность и отмаркировать
(указать номер исследуемого образца). Тестирование должно быть проведено в
течение 2 часов после вскрытия фольги!
4) Используя микропипетку и одноразовый наконечник, добавить
150 мкл охлажденной культуральной жидкости в круглую лунку для образца.
5) Считать результаты через 20 минут после добавления
образца.
Интерпретация
результатов
1) Результаты теста учитываются только при наличии четкой
красной линии в контрольной зоне (С) через 20 минут.
2) Образец считается положительным, если после 20 минут или
ранее красные линии образовались как в тестовых зонах (VT1) и/или (VT2), так и
в контрольной (С) зоне.
3) Образец считается отрицательным, если красная линия
отсутствует в тестовых зонах (VT1) и/или (VT2), но присутствует в контрольной
зоне (С).
4) Тест следует повторить, если красные линии отсутствуют
как в тестовых зонах (VT1) и/или (VT2), так и в контрольной зоне (С) через 20
минут.
Бульон
для индукции токсинов энтерогеморрагических E. coli
Принцип действия
Казаминовые кислоты и дрожжевой экстракт ускоряют рост
веротоксин-продуцирующих штаммов E. coli. Микроэлементы и высокое значение рН
также поддерживают синтез веротоксинов.
Состав среды (г/л) (CAYE-бульон
или аналог)
Казаминовые кислоты 20,0; дрожжевой экстракт 6,0; глюкоза
2,5; хлорид натрия 2,5; гидрофосфат калия двузамещенный 8,71; сульфат магния
0,05; хлорид марганца 0,005.
Приготовление
Растворить 7,95 г среды в 200 мл дистиллированной воды и
нагреть на кипящей водяной бане регулярно помешивая до полного растворения
среды. Автоклавировать при 121 °С 15 минут. Охладить среду до комнатной
температуры. В асептичных условиях добавить один флакон приготовленной добавки
(для индукции синтеза веротоксинов), перемешать; разлить по 1 мл при
перемешивании в стерильные пробирки. рН: 8,5 ± 0,2 при 25 °С. Приготовленный
бульон светло-коричневого цвета, прозрачный. Осадок, который иногда может
образоваться, не влияет на качество среды.
Проведение анализа
Отобрать 5 - 6 типичных колоний со среды выделения и
инокулировать в пробирки с бульоном. Инкубировать 6 часов при 37 °С без
перемешивания.
Контроль
качества
|
Тест-штаммы
|
Продукция веротоксинов
|
|
Escherichia coli O157:H7 43889
|
VT1 (-)
|
VT2 (+)
|
|
Escherichia coli О157.Н7 43890
|
VT1 (+)
|
VT2 (-)
|
|
Escherichia coli O157:H7 43888
|
VT1 (-)
|
VT2 (-)
|
|
Escherichia coli O157:H7 43885
|
VT1 (+)
|
VT2 (+)
|
Приложение 3
Инструкция
по применению набора реагентов для выявления специфических ДНК-маркеров
Escherichia coli О104:Н4 в бактериальных культурах и клиническом материале
1.
Назначение
Набор предназначен для выявления специфических ДНК-маркеров
Escherichia coli серотипа О104:Н4 в бактериальных культурах, клиническом
материале и пищевых продуктах методом полимеразной цепной реакции (ПЦР) с
электрофоретической детекцией продуктов амплификации в агарозном геле.
2.
Характеристика набора
Набор содержит компоненты, необходимые для проведения ПЦР, в
результате которой происходит амплификация специфических фрагментов ДНК
Escherichia coli серотипа О104:Н4 - генов stx2 (шига-токсина 2), rfb-О104,
контролирующего синтез первичных боковых цепей ЛПС (определяет серогруппу
О104), flicH4, определяющего синтез жгутикового антигена Н4.
В качестве внутреннего контроля используется дополнительная
пара праймеров на консервативную область гена 16S rRNA.
Это позволяет учесть возможное ингибирование реакции и исключить
ложно-отрицательный результат.
2.1. Принцип
действия
В основе метода лежит полимеразная цепная реакция с
использованием специфических олигонуклеотидных праймеров. Детекция продуктов
амплификации осуществляется электрофорезом в агарозном геле.
2.2.
Состав набора (на 100 реакций)
|
- ПЦР-буфер
|
- 2 пробирки по 1,2 мл
|
|
- Taq-POL (Taq I-полимераза)
|
- 40 мкл
|
|
- смесь Мульти О104
|
- 500 мкл
|
|
- dNTP (смесь
дезоксинуклеотидтрифосфатов)
|
- 50 мкл
|
|
- dH2O (деионизованная
вода)
|
- 400 мкл
|
|
- мин. масло (минеральное масло)
|
- 2,0 мл
|
|
- О104+ (положительный контроль)
|
- 100 мкл
|
3. Оборудование и материалы
ПЦР-бокс или отдельный стол, снабженный УФ-лампой
Твердотельный термостат или водяная баня
Набор автоматических пипеток переменного объема
Одноразовые наконечники для автоматических пипеток
Пробирки для микропроб объемом 1,5 мл
Пробирки для ПЦР на 0,5 мл или 0,2 мл
Вортекс-центрифуга
Центрифуга настольная
Термоциклер
Охладитель проб
Источник тока
Электрофорезная камера
Источник УФ
Весы лабораторные 2 класса точности
Холодильник бытовой с морозильной камерой
Отдельный халат и одноразовые перчатки
Емкость для сброса использованных наконечников
Вода дистиллированная
4.
Проведение анализа
4.1. Приготовление образцов для анализа в ПЦР: бактериальные
клетки суспендировать в 100 мкл стерильной дистиллированной воды до
концентрации 107 - 109 в пробирках 1,5 мл типа
«Эппендорф». Пробы прогреть при температуре 98 °С в течение 15 минут
(твердотельный термостат или водяная баня). Центрифугировать 5 минут при 2000 -
3000 g (4000 - 6000 об/мин.). Для многократного использования хранить при
температуре минус 20 °С.
Для приготовления образцов из клинического материала
использовать коммерческие наборы для выделения ДНК из клинического материала,
например, «ДНК-сорб-В», «ДНК-экспресс», следуя указаниям инструкции
изготовителя.
4.2 Проведение ПЦР
1. Перед проведением ПЦР-анализа внести
в одну или обе (в зависимости от объема исследования) пробирки «ПЦР-буфер» по
20 мкл фермента Taql-полимеразы из пробирки «Taq-POL». Полученной смеси
«ПЦР-буфер+» в каждой пробирке достаточно для проведения ПЦР-анализа 50
образцов. Смесь ПЦР-буфера с Taql-полимеразой «ПЦР-буфер+» можно хранить при
температуре +4 °С не более 6 мес. Отдельные компоненты «ПЦР-буфер» и «Taq-POL»
можно хранить при температуре минус 20 °С в течение 1 года.
2. Перенести содержимое пробирки «dNTP»
в пробирку «смесь Мульти О104». Полученную смесь «Мульти О104 с dNTP», рассчитанную на 100 реакций, можно хранить при
температуре +4 °С в течение 6 мес.
3. Включить охладитель проб (для охлаждения штативов с
пробирками можно использовать ледяные блоки).
4. В охлажденный штатив расставить ряд пробирок для ПЦР.
Количество пробирок должно соответствовать количеству анализируемых образцов с
учетом двух дополнительных пробирок, предназначенных для отрицательного и
положительного контролей.
5. Внести на дно каждой пробирки по 20 мкл смеси
«ПЦР-буфер+» (ПЦР-буфер с Taq I-полимеразой, п. 1).
6 Добавить во все пробирки по 5 мкл раствора «смесь Мульти
О104 с dNTP» (п. 2).
7. Добавить во все пробирки по одной капле (~20 - 30 мкл)
минерального масла. Если используется термоциклер с подогреваемой крышкой, то
минеральное масло не добавлять.
8. В пробирку для отрицательного контроля внести 5 мкл
деионизованной воды -
«dH2O«.
9. В пробирки для исследуемых образцов внести по 5 мкл
лизатов клеток или 5 мкл образцов, выделенных из клинических проб.
10. В пробирку для положительного контроля внести 5 мкл
раствора «О104+»
11. Все пробирки встряхнуть на вортексе, жидкость осадить на
дно пробирок кратковременным откручиванием на вортекс-центрифуге. Пробирки
поместить в блок термоциклера после прогрева прибора в режиме паузы при 95 °С
(режим горячего старта).
12. Провести реакцию амплификации по программе: 1-й цикл: 95
°С - 5 мин, 58 °С - 1 мин, 73 °С - 1 мин; далее 30 - 40 циклов: 94 °С - 30 сек,
60 °С - 30 сек, 72 °С - 30 сек; в конце: 1 цикл: 72 °С - 3 мин, 10 °С -
охлаждение (хранение). При тестировании лизатов клеток достаточно 25 - 30
циклов реакции.
13. После окончания реакции амплификации пробирки отправить
в комнату для анализа продуктов ПЦР. Пробы после амплификации можно хранить в
течение нескольких дней при 4 - 8 °С и несколько месяцев при минус 20 °С.
4.3 Анализ продуктов ПЦР
4.3.1 Приготовление агарозных гелей для электрофореза
Трис-боратный буфер (ТБЕ) для электрофореза: готовится
концентрированный (пятикратный) буфер 5xТБЕ (54 г Трис-осн., 27 г борной
кислоты, 20 мл 0,5 М ЭДТА, рН 8,0 растворяется в 1 л дистиллированной воды),
который разводится перед проведением анализа (к 200,0 мл 5xТБЕ добавить 800,0
мл дистиллированной воды).
Буфер для нанесения образцов (десятикратный): 0,025 г
бромфенолового синего; 4 мл глицерина; 5 мл 0,5 М ЭДТА, рН 8,0; довести до 10
мл дистиллированной водой.
Раствор 1,5% агарозы: взвесить 1,5 г агарозы, растворить в
100 мл ТБЕ буфера, поставить в кипящую водяную баню и выдержать 30 минут до
полного растворения агарозы. Для приготовления агарозы можно использовать СВЧ-печь.
Раствор охладить до 45 - 50 °С и залить необходимый гель (длина рабочей зоны
геля должна быть не менее 8 см). Агарозные гели можно приготовить за время
проведения реакции ПЦР.
4.3.2 Электрофорез в агарозном геле
Детекция продуктов амплификации осуществляется
электрофорезом в агарозном геле.
15 - 20 мкл реакционной смеси (ПЦР-продукт) из каждой
пробирки смешать с 2 мкл буфера для нанесения образцов, внести в лунки
агарозного геля и провести электрофорез при 10 в/см в течение 30 - 60 минут,
бромфеноловый краситель должен пройти до нижней границы геля. Гель окрасить в
водном растворе бромистого этидия (5 мкг/мл) в течение 30 минут, с последующей
20 минутной отмывкой в дистиллированной воде.
Внимание! Бромид этидия - канцерогенное соединение; работать
только в перчатках, избегать попадания на кожу и слизистые, при попадании на
кожу или слизистые тщательно промыть соответствующий участок водой.
Документация результатов проводится визуально при просмотре
геля на УФ-трансиллюминаторе с длиной волны 254 - 360 нм и фотографировании
гелей с использованием оранжевого светофильтра.
5.
Учет результатов
Результат ПЦР-анализа учитывается по наличию или отсутствию
на электрофореграмме специфических красно-оранжевых флюоресцирующих полос
амплифицированной ДНК.
Положительный контрольный образец ДНК. Сигнал от
положительного контроля виден как четыре фрагмента следующих размеров: 1250
п.н. (ген 16SrRNA), 480 п.н. (stx2-ген), 407 п.н. (ген
rfb-O104), 300 п.н. (ген flicH4) (рис. 1)
Отрицательный контрольный образец: в амплификате
отрицательного контрольного образца не должно наблюдаться красно-оранжевых
флюоресцирующих полос, соответствующих ампликонам положительного контроля.
Наличие таких полос свидетельствует о контаминации используемого набора
реагентов. В этом случае необходимо повторное исследование. При проведении ПЦР
белее 35 циклов возможно появление фрагмента 1250 п.н. гена 16S rRNA (следствие использования рекомбинантной Taq I-полимеразы).
Анализируемые клинические образцы:
- при наличии в пробе анализируемого образца ДНК E. coli
серотипа О104:Н4 в геле должны наблюдаться три красно-оранжевые флюоресцирующие
полосы специфических фрагментов ДНК размером 480 п.н. (stx2-ген), 407 п.н. (ген
rfb-О104) и 300 п.н. (ген flicH4), а также флюоресцирующая полоса, соответствующая
фрагменту 1250 п.н. гена 16S rRNA (внутренний контроль)
(рис. 1);
- при отсутствии в пробе анализируемого образца ДНК E. coli
серотипа О104:Н4 и наличии ДНК других бактерий в геле должна наблюдаться только
одна флюоресцирующая полоса, соответствующая фрагменту 1250 п.н. гена 16S rRNA (внутренний контроль);
- отсутствие флюоресцирующей полосы, соответствующей
фрагменту 1250 п.н. гена 16S rRNA, говорит об
ингибировании реакции и необходимости повторного исследования или об отсутствии
в данной пробе какой-либо бактериальной ДНК.
6.
Меры предосторожности
Организация работ на этапах приема, разбора и первичной
обработки материала, подготовки проб и выделения нуклеиновых кислот, а также
обеззараживания проб проводится в соответствии с требованиями СП
1.3.2322-08 «Безопасность работы с микроорганизмами III - IV групп
патогенности и гельминтами». Работа на остальных этапах ПЦР-анализа проводится
как с обеззараженным материалом.
7.
Условия хранения
Набор необходимо хранить при температуре 2 - 8 °С в течение
6 месяцев.
Транспортирование: при температуре от 2 °С до 8 °С.
Приложение 4
Инструкция
по применению набора реагентов латексной диагностики для быстрой идентификации
шига-токсинпродуцирующего штамма Escherichia coli O104:H4
1.
Назначение и характеристика тест-системы
Латексная тест-система Е. coli О104:Н4 предназначена для
экспресс-выявления и идентификации микробных клеток Escherichia coli О104:Н4
при проведении лабораторных исследований и представляет собой набор из трех
флаконов емкостью 5 мл.
Латексная тест-система Е. coli О104:Н4 обеспечивает
типоспецифическое выявление и идентификацию микробных клеток Е. coli O104:H4 в
суспензиях, полученных из колоний микроорганизмов, выращенных на пластинках
ГРМ-агара. Специфическими мишенями данного теста являются липополисахарид О104
и жгутиковый антиген Н4.
2.
Состав тест-системы
В состав «латексной тест-системы Е. coli O104:H4» входят:
- флакон 1 (латексный тест), содержит 0,5 % взвеси частиц
монодисперсного полистирольного альдегидного латекса диаметром 0,65 мкм,
сенсибилизированного иммуноглобулинами G, выделенными из сывороток крови кроликов,
содержащих антитела к липополисахариду О104 и жгутиковому антигену Н4 Е. coli
O104:H4;
- флакон 2 (контрольный тест), содержит 0,5% взвеси частиц
монодисперсного полистирольного альдегидного латекса, сенсибилизированного
иммуноглобулинами из сывороток крови не иммунизированных кроликов;
- флакон 3 (позитивный контроль), содержит инактивированную
нагреванием взвесь культуры Е. coli О104:Н4, концентрация 10 единиц по ОСО
42-28-85 П.
3.
Принцип действия
Микробные клетки Е. coli O104:H4, присутствующие в
исследуемой пробе, взаимодействуют с латексными частицами, сенсибилизированными
антителами против липополисахаридого антигена О104 и жгутикового антигена Н4 с
последующим образованием видимых агглютинатов.
4.
Меры предосторожности
Подготовку материала для исследования проводят с соблюдением
специальной техники безопасности в соответствии с СП
1.3.2322-08 «Безопасность работы с микроорганизмами III - IV групп
патогенности и возбудителями паразитарных болезней».
5.
Проведение анализа
5.1.
Материалы и оборудование
- 0,01 моль натрий-фосфатный буфер, рН 7,4 (ФБР);
- механические дозаторы переменного объема, позволяющие
отбирать объемы жидкости 0,1; 0,01 и 0,005 мл;
- предметные стекла;
- стеклянные палочки.
5.2.
Анализируемые образцы
5.2.1. Подозрительные колонии микроорганизмов, выращенные на
пластинках ГРМ-агара в аэрофильных условиях в течение 18 - 24 часов при
температуре 37 °С.
Примечание - Анализируемые образцы не подвергать
автоклавированию.
5.3.
Анализ
5.3.1. На предметное стекло нанести 20 мкл физиологического раствора,
стеклянной палочкой снять часть колонии тестируемого штамма (исследуемый
образец) и растереть в капле физиологического раствора до получения гомогенной
суспензии.
5.3.2. Извлечь необходимое количество упаковок латексной
тест-системы из холодильника и выдержать при комнатной температуре 20 минут.
Примечание - перед применением латексный тест тщательно
суспендировать до гомогенного состояния.
5.3.3. К исследуемому образцу
механическим дозатором нанести на предметное стекло 0,015 мл латексного теста (флакон
№ 1) и оба компонента осторожно перемешать стеклянной палочкой до получения
гомогенной суспензии. Реакционную смесь на стекле инкубировать при комнатной
температуре 2 минуты, периодически покачивая, а затем регистрировать результаты
реакции.
5.3.4. Проверка качества
контрольного теста. К 0,02 мл исследуемого образца, нанесенного на предметное
стекло, добавить 0,015 мл контрольного теста (флакон № 2) и оба компонента
осторожно перемешать стеклянной палочкой до получения гомогенной суспензии.
Реакционную смесь на стекле инкубировать при комнатной температуре 2 минуты,
периодически покачивая, а затем регистрировать результаты реакции.
5.3.5. Контроль специфичности
латексного теста. К 0,02 мл позитивного контроля (флакон № 3), нанесенного на
предметное стекло, добавить 0,015 мл латексного теста (флакон № 1) и оба
компонента осторожно перемешать стеклянной палочкой до получения гомогенной
суспензии. Реакционную смесь на стекле инкубировать при комнатной температуре 2
минуты, периодически покачивая, а затем регистрировать результаты реакции.
6.
Регистрация и учет результатов
Учет результатов по п. 5.3.3, 5.3.4
и 5.3.5 провести через 2 минуты,
руководствуясь таблицей.
Таблица
1
Интерпретация
результата
|
Положительный
результат
|
Наличие
видимой четкой окрашенной агглютинации частиц при добавлении к исследуемому
образцу латексного теста (флакон 1).
Наличие
видимой четкой окрашенной агглютинации частиц при добавлении к позитивному
контролю (флакон 3) латексного теста (флакон 1).
Отсутствие
агглютинации, фон равномерно мутный при добавлении к исследуемому образцу
контрольного теста (флакон 2).
|
|
Отрицательный
результат
|
Отсутствие
агглютинации, фон равномерно мутный при добавлении к исследуемому образцу
латексного теста (флакон 1).
Наличие
видимой четкой окрашенной агглютинации частиц при добавлении к позитивному
контролю (флакон 3) латексного теста (флакон 1).
|
|
Тест
не работает
|
Отсутствие
агглютинации, фон равномерно мутный при добавлении к позитивному контролю
(флакон 3) латексного теста (флакон 1).
|
7.
Условия хранения и эксплуатации латексной тест-системы
Набор реагентов тест-системы необходимо хранить в герметично
закрытых флаконах в сухом защищенном от света месте при температуре 2 - 8 °С.
Допускается транспортировка набора реагентов при температуре 2 - 25 °С в срок
не более 7 суток.
Примечание - Не замораживать.
Срок годности - 1 год. Для получения надежных результатов
необходимо строгое соблюдение настоящей инструкции по применению.
Приложение 5
Определение чувствительности культур Е. coli к
антибиотикам
Чувствительность штаммов E. coli к антибиотикам диско-диффузионным
методом (ДДМ или методом дисков) определяют согласно Методическим указаниям МУК
4.2.1890-04 «Определение чувствительности микроорганизмов к антибактериальным
препаратам»
Принцип
метода
ДДМ определения чувствительности микроорганизмов к антибиотикам
основан на способности антибактериальных препаратов (АБП) диффундировать из
пропитанных ими бумажных дисков в питательную среду, угнетая рост
микроорганизмов, посеянных на поверхности агара.
Приготовление
питательных сред для определения чувствительности
Для оценки чувствительности культуры E. coli к антибиотикам
необходимо использовать только специально предназначенные для этой цели среды.
Каждую партию плотных питательных сред перед применением необходимо проверять
на пригодность для роста тестируемых микроорганизмов. Для этого используются
соответствующие контрольные штаммы, например, E. coli АТСС 25922 или E. coli
ATCC 38218. Внутрилабораторный контроль качества среды необходимо проводить при
использовании всех известных коммерчески доступных питательных сред, независимо
от их производителя.
Выбранная питательная среда для определения чувствительности
готовится из сухой среды промышленного производства в соответствии с
инструкцией изготовителя. После автоклавирования питательную среду охлаждают до
48 - 50 °С и разливают по чашкам слоем толщиной 4 мм (на чашку диаметром 100 мм
25 мл агара, на чашку диаметром 90 мм - 20 мл). Чашки оставляют при комнатной
температуре для застывания агара. Приготовленные указанным образом питательные
среды предпочтительнее использовать немедленно. Допускается хранение в
запаянных полиэтиленовых пакетах в холодильнике при +4 - +8 °С в течение 5
суток.
Контроль
качества питательных сред, используемых для определения чувствительности E.
coli к антибиотикам
Контроль роста
Из суточной культуры E. coli ATCC 25922 или E. coli ATCC
38218 (или другой культуры) готовят микробную взвесь, соответствующую по
плотности 0,5 по стандарту МакФарланда (содержащую приблизительно 1,5×108
КОЕ/мл), затем из этой взвеси готовят серию последовательных десятикратных
разведений. На приготовленные чашки с проверяемой средой высевают по 0,1 мл
взвеси -5, -6, -7 разведений, содержащих соответственно 1×103,
1×102, 1×101 КОЕ/мл. При хороших питательных
свойствах среды должен отмечаться рост микроорганизмов из -6, -7 разведений.
Интегральный
контроль качества определения чувствительности
Наиболее доступным интегральным методом оценки качества
определения чувствительности патогенов к антибиотикам является сопоставление
результатов определения чувствительности (диаметров зон подавления роста)
контрольных (референтных) штаммов микроорганизмов с соответствующими
показателями, приведенными в их паспортной характеристике. Тестирование
контрольных штаммов проводят в соответствии с описанными выше методами, параллельно
тестированию клинических изолятов.
Диски
с антибиотиками
Для получения правильных результатов определения
чувствительности ДДМ необходимо строго соблюдать правила хранения и
использования коммерческих дисков, в противном случае содержание в них антибиотиков
может снизиться ниже допустимого уровня (прежде всего в результате увлажнения)
еще до истечения срока годности.
Долговременное хранение дисков с АБП осуществляется в
герметичной упаковке в морозильной камере при температуре -18 °С и ниже. Небольшие
партии дисков, используемые при повседневной работе, можно хранить в
холодильнике при температуре +4 - +8 °С, плотно укупоренными так, чтобы
гарантировать невозможность попадания во флакон влаги, кроме того для
дополнительной защиты от влаги во флаконах (картриджах) с дисками коммерческого
изготовления содержится специальный влагопоглотитель (силикагель).
Флаконы (картриджи) с дисками следует извлекать из
холодильника за 1 ч до начала работы и выдерживать герметично закрытыми до
достижения ими комнатной температуры, что предотвращает образование конденсата
на дисках после открывания флаконов.
Внимание! Для получения достоверных результатов используйте
диски отечественных производителей на средах АГВ или типа АГВ производства
филиала «Питательные среды г. Махачкала ООО «Микроген» и ФБУН ГНЦПМБ, а среду
Мюллер-Хинтона только с импортными дисками.
Приготовление
бактериальной суспензии и инокуляция
При определении чувствительности ДДМ используют стандартный
инокулюм, соответствующий по плотности 0,5 по стандарту МакФарланда и
содержащий примерно 1,5 × 108 КОЕ/мл. Инокулюм следует
использовать в течение 15 минут после приготовления. Для засева приготовленных
чашек с питательной средой стандартный инокулюм наносят пипеткой на поверхность
агаровой пластинки чашки Петри в объеме 1 - 2 мл, равномерно распределяют
взвесь микроорганизмов по поверхности питательной среды покачиванием, после
чего удаляют избыток инокулюма пипеткой. Приоткрытые чашки подсушивают при
комнатной температуре в течение 10 - 15 мин.
Аппликация
дисков и инкубация
Не позднее, чем через 15 мин после инокуляции тестируемого
микроба на поверхность питательной среды наносят диски с АБП. Аппликацию дисков
проводят с помощью стерильного пинцета или автоматического диспенсера. Расстояние
от диска до края чашки и между дисками должно быть 15 - 20 мм. Таким образом,
на одну чашку диаметром 100 мм следует помещать не более 6 дисков с АБП. Диски
должны равномерно контактировать с поверхностью агара, для чего их следует
аккуратно прижать пинцетом.
Непосредственно после аппликации дисков чашки Петри с
посевами помещают в термостат и инкубируют при температуре 37 °С в течение 18 -
24 ч. Увеличение интервала времени между нанесением дисков на поверхность среды
и началом инкубации (а соответственно - началом роста исследуемой культуры
микроорганизма) приводит к «преддиффузии» АБП в агар и к увеличению диаметра
зоны подавления роста.
Учет
результатов
После окончания инкубации чашки помещают кверху дном на
темную матовую поверхность так, чтобы свет падал на них под углом в 45° (учет в
отраженном свете). Диаметр зон задержки роста измеряют с точностью до 1 мм,
предпочтительнее пользоваться штангенциркулем или кронциркулем.
При измерении зон задержки роста испытуемой культуры следует
учитывать лишь зону полного подавления видимого роста бактерий. Не следует
обращать внимания на очень мелкие колонии, выявляемые в пределах зоны задержки
роста тестируемого микроба только при особых условиях освещения или увеличении,
и едва заметный налет у края зоны.
Крупные колонии, выявляемые в пределах четкой зоны
подавления роста тестируемого микроба, свидетельствуют о наличии посторонней
микрофлоры или о гетерорезистентности популяции микроорганизмов, в этом случае
необходимо повторить идентификацию микроорганизма, формирующего эту колонию, и
определение чувствительности этого штамма.
В таблице приведена антибиотикограмма штамма E. coli O104:H4
и интерпретация результатов определения чувствительности E. coli к антибиотикам
по величине зон подавления роста испытуемого штамма.
__________________
* - для фосфомицина в
питательную среду необходимо добавить глюкозо-6-фосфат до концентрации 25
мкг/мл
Приложение 6
Инструкция
по применению иммунохроматографического экспресс-теста для определения
энтерогеморрагических E. coli О157
Принцип работы иммунохроматографического теста основан на
взаимодействии антигенов, находящихся в образце исследуемого материала с
антителами, меченными золотом (Singlepath E. coli О157 или аналог).
Иммунохроматографический тест представляет собой
диагностическую тест-панель с круглой лункой для добавления образца, овальным
окном с тестовой (Т) и контрольной (С) зонами.
1) Образец добавляется в круглую лунку.
2) Образец адсорбируется подложкой и взаимодействует со
специфичными к E. coli О157 антителами мечеными золотом.
3) В присутствии антигенов E. coli О157 образуется комплекс
с мечеными антителами, который мигрирует до зоны связывания в тестовой зоне (Т).
4) Зона связывания (Т) содержит антитела к комплексу
антиген-антитело. В результате образуется четкая красная линия.
5) Оставшийся образец продолжает движение к контрольной зоне
(С) и образует четкую красную линию, указывающую на то, что тест работает
правильно.
Чувствительность метода - 1 клетка (КОЕ) E. coli О157 в 25 г
образца.
Ограничения метода
1) На результат не влияет наличие сопутствующих
микроорганизмов.
Условия
хранения
Иммунохроматографический тест для определения E. coli О157
стабилен до даты, указанной на упаковке, при хранении в условиях +2 - 8 °С.
Проведение
анализа
1. Смешать 25 г (мл) образца с 225 мл среды обогащения.
Выбор среды обогащения зависит от типа продукта. Среда для молочных продуктов -
модифицированный триптиказо-соевый бульон с новобиоцином. Среда для мясных
продуктов - модифицированный бульон ЕС с новобиоцином. При необходимости
гомогенизировать образец.
2. Инкубировать 18 - 24 ч при 37 °С.
3. Перенести примерно 1 - 2 мл культуральной жидкости в
полипропиленовую (или стеклянную) пробирку и инкубировать на кипящей водяной
бане 15 мин.
4. Дать остыть пробе до комнатной температуры.
Проведение
тестирования
1. Перед использованием обогащенный образец и
иммунохроматографический тест должны быть комнатной температуры (обычно тесты
хранятся в холодильнике).
2. Вскрыть пакет из фольги, в который упакован тест.
3. Положить тест на ровную поверхность и отмаркировать
(указать номер исследуемого образца). Тестирование должно быть проведено в
течение 2 часов после вскрытия фольги!
4. Используя микропипетку и одноразовый наконечник, добавить
150 мкл термически инактивированной и охлажденной культуральной жидкости в
круглую лунку для образца.
5. Считать результаты через 20 минут после добавления
образца.
Интерпретация
результатов
1. Результаты теста учитываются только при наличии четкой
красной линии в контрольной зоне (С) через 20 минут.
2. Образец считается положительным, если после 20 минут или
ранее красные линии образовались как в тестовой (Т), так и в контрольной (С)
зоне.
3. Образец считается отрицательным, если красная линия
отсутствует в тестовой зоне (Т), но присутствует в контрольной зоне (С).
4. Тест следует повторить, если красные линии отсутствуют
как в тестовой, так и в контрольной зоне через 20 минут.
Приложение 7
Инструкция
по применению набора реагентов для выявления специфических участков ДНК
энтерогеморрагических Escherichia Coli О157 в бактериальных культурах и
клиническом материале
1.
Назначение
Набор предназначен для выявления специфических участков ДНК
энтерогеморрагических Escherichia coli в бактериальных культурах, клиническом
материале и пищевых прокуктах методом полимеразной цепной реакции (ПЦР) с
электрофоретической детекцией продуктов амплификации в агарозном геле.
2.
Характеристика набора
Набор содержит компоненты, необходимые для проведения ПЦР, в
результате которой происходит амплификация фрагментов генов интимина (eaeА),
шига-токсина 1 (stx1), шига-токсина 2 (stx2), гена rfb, контролирующего синтез
первичных боковых цепей ЛПС (определяют серогруппу О157). Получаемая в
результате ПЦР комбинация из этих фрагментов позволяет выявлять и
дифференцировать различные токсин-продуцирующие штаммы энтерогеморрагических Е.
coli.
В качестве внутреннего контроля используется дополнительная
пара праймеров на консервативную область гена 16S rRNA.
Это позволяет учесть возможное ингибирование реакции и исключить
ложно-отрицательный результат.
2.1.
Принцип действия
В основе метода лежит полимеразная цепная реакция с
использованием специфических олигонуклеотидных праймеров. Детекция продуктов
амплификации осуществляется электрофорезом в агарозном геле.
2.2.
Состав набора (на 100 реакций)
|
- ПЦР-буфер
|
- 2 пробирки по 1,2 мл
|
|
- Taq-POL (Taq I-полимераза)
|
- 40 мкл
|
|
- смесь Мульти О157
|
- 500 мкл
|
|
- dNTP (смесь
дезоксинуклеотидтрифосфатов)
|
- 50 мкл
|
|
- dH2O (деионизованная
вода)
|
- 400 мкл
|
|
- мин. масло (минеральное масло)
|
- 2,0 мл
|
|
- О157 + (положительный контроль)
|
- 100 мкл
|
3.
Оборудование и материалы
ПЦР-бокс или отдельный стол, снабженный УФ-лампой
Твердотельный термостат или водяная баня
Два набора автоматических пипеток переменного объема
Одноразовые наконечники для автоматических пипеток
Пробирки для микропроб объемом 1,5 мл
Пробирки для ПЦР на 0,5 мл или 0,2 мл
Вортекс-центрифуга
Центрифуга настольная
Термоциклер
Охладитель проб
Источник тока
Электрофорезная камера
Источник УФ
Весы лабораторные 2 класса точности
Холодильник бытовой с морозильной камерой
Отдельный халат и одноразовые перчатки
Емкость для сброса использованных наконечников
Вода дистиллированная
4.
Проведение анализа
4.1. Приготовление образцов для анализа в ПЦР: бактериальные
клетки суспендировать в 100 мкл стерильной дистиллированной воды до
концентрации 107 - 109 в пробирках 1,5 мл типа
«Эппендорф». Пробы прогреть при температуре 98 °С в течение 15 минут
(твердотельный термостат или водяная баня). Центрифугировать 5 минут при 2000 -
3000 g (4000 - 6000 об/мин.). Для многократного использования хранить при температуре
минус 20 °С.
Для приготовления образцов из клинического материала
использовать коммерческие наборы для выделения ДНК из клинического материала.
4.2 Проведение ПЦР
1. Перед проведением ПЦР-анализа внести в одну или обе (в
зависимости от объема исследования) пробирки «ПЦР-буфер» по 20 мкл фермента
Taql-полимеразы из пробирки «Taq-POL». Полученной смеси «ПЦР-буфер+» в каждой
пробирке достаточно для проведения ПЦР-анализа 50 образцов. Смесь ПЦР-буфера с
Taql-полимеразой «ПЦР-буфер+» можно хранить при температуре + 4 °С не более 6
мес. Отдельные компоненты «ПЦР-буфер» и «Taq-POL» можно хранить при минус 20 °С
в течение 1 года.
2. Перенести содержимое пробирки «dNTP»
в пробирку «смесь Мульти О157». Полученную смесь «Мульти О157 с dNTP», рассчитанную на 100 реакций, можно хранить при
температуре + 4 °С в течение 6 мес.
3. Включить охладитель проб (для охлаждения штативов с
пробирками можно использовать ледяные блоки).
4. В охлажденный штатив расставить ряд пробирок для ПЦР (0,5
мл). Количество пробирок должно соответствовать количеству анализируемых
образцов с учетом двух дополнительных пробирок, предназначенных для
отрицательного и положительного контролей.
5. Внести на дно каждой пробирки по 20 мкл смеси
«ПЦР-буфер+» (ПЦР-буфер с Taq I-полимеразой, п. 1).
6. Добавить во все пробирки по 5 мкл раствора «смесь Мульти
О157 с dNTP» (п. 2).
7. Добавить во все пробирки по одной капле (~20 мкл)
минерального масла. Если используется термоциклер с подогреваемой крышкой, то
минеральное масло не добавлять.
8. В пробирку для отрицательного контроля внести 5 мкл
деионизованной воды -
«dH2O«.
9. В пробирки для исследуемых образцов внести по 5 мкл
лизатов клеток или 5 мкл образцов, выделенных из клинических проб.
10. В пробирку для положительного контроля внести 5 мкл
раствора «О157+»
11. Все пробирки встряхнуть на вортексе, жидкость осадить на
дно пробирок кратковременным откручиванием на вортекс-центрифуге. Пробирки
поместить в блок термоциклера после прогрева прибора в режиме паузы при 95 °С
(режим горячего старта).
12. Провести реакцию амплификации по программе: 1-й цикл: 95
°С - 5 мин, 58 °С - 1 мин, 73 °С - 1 мин; далее 30 - 40 циклов: 94 °С - 30 сек,
60 °С - 30 сек, 72 °С - 30 сек; в конце: 1 цикл: 72 °С - 3 мин, 10 °С -
охлаждение (хранение). При тестировании лизатов клеток достаточно 30 циклов
реакции.
13. После окончания реакции амплификации пробирки отправить
в комнату для анализа продуктов ПЦР. Пробы после амплификации можно хранить в
течение нескольких дней при 4 - 8 °С и несколько месяцев при минус 20 °С.
4.3 Анализ продуктов ПЦР
4.3.1 Приготовление агарозных гелей для электрофореза
Трис-боратный буфер (ТБЕ) для электрофореза: готовится
концентрированный (пятикратный) буфер 5xТБЕ (54 г Трис-осн., 27 г борной
кислоты, 20 мл 0,5 М ЭДТА, рН 8,0 растворяется в 1 л дистиллированной воды),
который разводится перед проведением анализа (к 200,0 мл 5xТБЕ добавить 800,0
мл дистиллированной воды).
Буфер для нанесения образцов (десятикратный): 0,025 г
бромфенолового синего; 4 мл глицерина; 5 мл 0,5 М ЭДТА, рН 8,0; довести до 10
мл дистиллированной водой.
Раствор 1,5% агарозы: взвесить 1,5 г агарозы, растворить в
100 мл ТБЕ буфера, поставить в кипящую водяную баню и выдержать 30 минут до
полного растворения агарозы. Для приготовления агарозы можно использовать
СВЧ-печь. Раствор охладить до 45 - 50 °С и залить необходимый гель (длина
рабочей зоны геля должна быть не менее 8 см). Агарозные гели можно приготовить
за время проведения реакции ПЦР.
4.3.2 Электрофорез в агарозном геле
Детекция продуктов амплификации осуществляется
электрофорезом в агарозном геле.
15 - 20 мкл реакционной смеси (ПЦР-продукт) из каждой
пробирки смешать с 2 мкл буфера для нанесения образцов, внести в лунки
агарозного геля и провести электрофорез при 10 в/см в течение 30 - 60 минут,
бромфеноловый краситель должен пройти до нижней границы геля. Гель окрасить в
водном растворе бромистого этидия (5 мкг/мл) в течение 30 минут, с последующей
20 минутной отмывкой в дистиллированной воде.
Внимание! Бромид этидия - канцерогенное соединение; работать
только в перчатках, избегать попадания на кожу и слизистые, при попадании на
кожу или слизистые тщательно промыть соответствующий участок водой.
Документация результатов проводится визуально при просмотре геля на
УФ-трансиллюминаторе с длиной волны 254 - 360 нм и фотографировании гелей с
использованием оранжевого светофильтра.
5.
Учет результатов
Результат ПЦР-анализа учитывается по наличию или отсутствию
на электрофореграмме специфических красно-оранжевых флюоресцирующих полос
амплифицированной ДНК.
Положительный контрольный образец ДНК. Сигнал от
положительного контроля виден как пять фрагментов следующих размеров: 1250 п.н.
(ген 16S rRNA), 690 п.н. - (еае-ген), 480 п.н. -
(stxII-ген), 400 п.н. - (rfb-ген), 330 п.н. - (stxI-ген) (рис. 1).
Отрицательный контрольный образец: в амплификате
отрицательного контрольного образца не должно наблюдаться красно-оранжевых
флюоресцирующих полос, соответствующих ампликонам положительного контроля.
Наличие таких полос свидетельствует о контаминации используемого набора реагентов.
В этом случае необходимо повторное исследование. При проведении ПЦР белее 35
циклов возможно появление фрагмента 1250 п.н. гена 16S rRNA
(следствие использования рекомбинантной Taq I-полимеразы).
Анализируемые образцы.
- при наличии в пробе анализируемого образца ДНК возбудителя
геморрагического колита в геле должны наблюдаться четыре красно-оранжевые
флюоресцирующие полосы специфических фрагментов ДНК размером 690 п.н. - (ген
еае), 480 п.н. - (ген stx2), 400 п.н. - (ген rfb) и 330 п.н. - (ген stx1), а также
флюоресцирующая полоса, соответствующая фрагменту 1250 п.н. гена 16S rRNA (внутренний контроль) (рис. 1);
- при отсутствии в пробе анализируемого образца ДНК
шига-токсин содержащих E. coli серогруппы О157 и наличии ДНК бактерий других
видов в геле должна наблюдаться только одна флюоресцирующая полоса,
соответствующая фрагменту 1250 п.н. гена 16S rRNA
(внутренний контроль);
- отсутствие флюоресцирующей полосы, соответствующей
фрагменту 1250 п.н. гена 16S rRNA, говорит об
ингибировании реакции и необходимости повторного исследования или об отсутствии
в данной пробе какой-либо бактериальной ДНК.
6.
Меры предосторожности
Организация работ на этапах приема, разбора и первичной
обработки материала, подготовки проб и выделения нуклеиновых кислот, а также
обеззараживания проб проводится в соответствии с требованиями СП
1.3.2322-08 «Безопасность работы с микроорганизмами III - IV групп
патогенности и гельминтами». Работа на остальных этапах ПЦР-анализа проводится
как с обеззараженным материалом.
7.
Условия хранения и эксплуатации набора
Набор необходимо хранить при температуре 2 - 8 °С в течение
6 месяцев.
Транспортирование: при температуре от 2 °С до 8 °С.
Приложение 8
Инструкция
по применению набора реагентов латексной диагностики для быстрой идентификации
возбудителя геморрагического колита Escherichia coli О157:H7
1.
Назначение и характеристика тест-системы
Тест-система для экспресс-выявления и идентификации
микробных клеток Escherichia coli О157:Н7 при проведении лабораторных
исследований и представляет собой набор из трех флаконов емкостью 5 мл.
Тест-система обеспечивает типоспецифическое выявление и
идентификацию микробных клеток Е. coli О157:H7 в суспензиях, полученных из
колоний микроорганизмов, выращенных на пластинках ГРМ-агара. Специфическими
мишенями данного теста являются липополисахарид О157 и жгутиковый антиген Н7 Е.
coli О157:H7.
2.
Состав тест-системы
В состав тест-системы входят:
- флакон 1 (латексный тест), содержит 0,5% взвеси частиц
монодисперсного полистирольного альдегидного латекса диаметром 0,65 мкм,
сенсибилизированного иммуноглобулинами G, выделенными из сывороток крови
кроликов, содержащих антитела к липополисахариду О157 и жгутиковому антигену Н7
Е. coli О157:H7;
- флакон 2 (контрольный тест), содержит 0,5% взвеси частиц
монодисперсного полистирольного альдегидного латекса, сенсибилизированного
иммуноглобулинами из сывороток крови не иммунизированных кроликов;
- флакон 3 (позитивный контроль), содержит инактивированную
нагреванием взвесь культуры Е. coli О157:Н7, концентрация 10 единиц по ОСО
42-28-85 П.
3.
Принцип действия
Микробные клетки Е. coli О157:H7, присутствующие в
исследуемой пробе, взаимодействуют с латексными частицами, сенсибилизированными
антителами против липополисахаридого антигена О157 и жгутикового антигена Н7 с
последующим образованием видимых агглютинатов.
4.
Меры предосторожности
Подготовку материала для исследования проводят с соблюдением
специальной техники безопасности в соответствии с СП
1.3.2322-08 «Безопасность работы с микроорганизмами I - IV групп
патогенности и возбудителями паразитарных болезней».
5.
Проведение анализа
5.1.
Материалы и оборудование
- 0,01 моль натрий-фосфатный буфер, рН 7,4 (ФБР);
- механические дозаторы переменного объема, позволяющие
отбирать объемы жидкости 0,1; 0,01 и 0,005 мл;
- предметные стекла;
- стеклянные палочки.
5.2.
Анализируемые образцы
5.2.1. Подозрительные колонии микроорганизмов, выращенные на
пластинках ГРМ-агара в аэрофильных условиях в течение 18 - 24 часов при
температуре 37 °С.
Примечание - Анализируемые образцы не подвергать
автоклавированию.
5.3.
Анализ
5.3.1. На предметное стекло нанести 20 мкл физиологического
раствора, стеклянной палочкой снять часть колонии тестируемого штамма
(исследуемый образец) и растереть в капле физиологического раствора до
получения гомогенной суспензии.
5.3.2. Извлечь необходимое количество упаковок латексной тест-системы
из холодильника и выдержать при комнатной температуре 20 минут.
Примечание - перед применением латексный тест тщательно
суспендировать до гомогенного состояния.
5.3.3. К исследуемому образцу
механическим дозатором нанести на предметное стекло 0,015 мл латексного теста
(флакон № 1) и оба компонента осторожно перемешать стеклянной палочкой до
получения гомогенной суспензии. Реакционную смесь на стекле инкубировать при
комнатной температуре 2 минуты, периодически покачивая, а затем регистрировать результаты
реакции.
5.3.4. Проверка качества
контрольного теста. К 0,02 мл исследуемого образца, нанесенного на предметное
стекло, добавить 0,015 мл контрольного теста (флакон № 2) и оба компонента
осторожно перемешать стеклянной палочкой до получения гомогенной суспензии.
Реакционную смесь на стекле инкубировать при комнатной температуре 2 минуты,
периодически покачивая, а затем регистрировать результаты реакции.
5.3.5. Контроль специфичности
латексного теста. К 0,02 мл позитивного контроля (флакон № 3), нанесенного на
предметное стекло, добавить 0,015 мл латексного теста (флакон № 1) и оба
компонента осторожно перемешать стеклянной палочкой до получения гомогенной
суспензии. Реакционную смесь на стекле инкубировать при комнатной температуре 2
минуты, периодически покачивая, а затем регистрировать результаты реакции.
6.
Регистрация и учет результатов
Учет результатов по п. 5.3.3, 5.3.4
и 5.3.5 провести через 2 минуты,
руководствуясь таблицей.
Таблица
1
Интерпретация
результата
|
Положительный
результат
|
Наличие
видимой четкой окрашенной агглютинации частиц при добавлении к исследуемому образцу
латексного теста (флакон 1).
Наличие
видимой четкой окрашенной агглютинации частиц при добавлении к позитивному
контролю (флакон 3) латексного теста (флакон 1).
Отсутствие
агглютинации, фон равномерно мутный при добавлении к исследуемому образцу контрольного
теста (флакон 2).
|
|
Отрицательный
результат
|
Отсутствие
агглютинации, фон равномерно мутный при добавлении к исследуемому образцу
латексного теста (флакон 1).
Наличие
видимой четкой окрашенной агглютинации частиц при добавлении к позитивному контролю
(флакон 3) латексного теста (флакон 1).
|
|
Тест
не работает
|
Отсутствие
агглютинации, фон равномерно мутный при добавлении к позитивному контролю
(флакон 3) латексного теста (флакон 1).
|
7.
Условия хранения и эксплуатации латексной тест-системы
Набор реагентов тест-системы необходимо хранить в герметично
закрытых флаконах в сухом защищенном от света месте при температуре 2 - 8 °С.
Допускается транспортировка набора реагентов тест-системы при температуре 2 -
25 °С в срок не более 7 суток.
Примечание - Не замораживать.
Срок годности - 1 год. Для
получения надежных результатов необходимо строгое соблюдение настоящей
инструкции по применению.
|
Руководитель
Федеральной службы по надзору в сфере защиты прав потребителей и благополучия
человека, Главный государственный санитарный врач Российской Федерации
|
Г.Г.
Онищенко
|
Содержание
Новости
Библиотека
Soft по ОТ и ПБ
Консультации
Агрегатор
Услуги
Форум
Золотой фонд
ССОТ
CHAT-OT


.webp)




