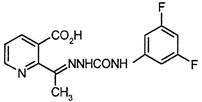
Измерения концентраций дифлуфензопира выполняют методом
высокоэффективной жидкостной хроматографии (ВЭЖХ) на обращенной фазе с
ультрафиолетовым детектором.
Концентрирование вещества из воздуха осуществляют на
бумажный фильтр, экстракцию с фильтров выполняют смесью этанол-вода (8:2, по
объему). Смыв е кожных покровов проводят этиловым спиртом.
Нижний предел измерения в анализируемом объеме пробы - 2 нг.
Средняя полнота извлечения с фильтров - 96,25 %, с поверхности кожи - 82,07 %.
|
Жидкостный хроматограф с
ультрафиолетовым детектором с переменной длиной волны
|
|
|
Барометр-анероид с диапазоном
измерения атмосферного давления 5 - 790 мм рт. ст.
|
ТУ 2504-1797-75
|
|
Весы аналитические с пределом
взвешивания 110 г и пределом допустимой погрешности 0,001 г
|
ГОСТ
Р 53228-08
|
|
Гигрометр психометрический с
диапазоном измерений относительной влажности от 30 до 90 %
|
ТУ 25-11-1645-84
|
|
Колбы мерные 2-100-2 и 2-1000-2
|
ГОСТ
1770-74
|
|
Меры массы
|
ГОСТ
OIML R 111-1-09
|
|
Пипетки градуированные 2-го класса
точности вместимостью 1,0; 2,0; 5,0; 10 см3
|
ГОСТ
29227-91
|
|
Пробоотборное устройство
2-канальное, с диапазонами расхода 0,2 - 1,0 дм3/мин и 5,0 - 1,0
дм3/мин и пределом допустимой погрешности ±7 %
|
|
|
Термометр лабораторный шкальный
ТЛ-11, цена деления 1 °С, пределы измерения - 35 - 55 °С
|
ТУ 25-2021.055-83
|
|
Цилиндры мерные 2-го класса
точности вместимостью 100, 500 и 1000 см3
|
ГОСТ
1770-74
|
Примечание. Допускается использование средств измерения с
аналогичными или лучшими характеристиками.
|
Дифлуфензопир, аналитический
стандарт с содержанием основного компонента 97,6 %
|
|
|
Ацетонитрил для хроматографии, хч
|
ТУ 6-09-14.2167-84
|
|
Вода для лабораторного анализа
(бидистиллированная или деионизованная)
|
ГОСТ
Р 52501-05
|
|
Калий марганцовокислый
(перманганат калия), хч
|
ГОСТ
20490-75
|
|
Калий углекислый (карбонат калия,
поташ), хч, прокаленный
|
ГОСТ
4221-76
|
|
Кислота муравьиная, 85 %
|
ГОСТ
5848-73
|
|
Кислота ортофосфорная
|
|
|
Метиловый спирт (метанол), хч
|
ГОСТ 6995-77
|
|
Натрий углекислый (карбонат
натрия), хч
|
ГОСТ
83-79
|
|
Спирт этиловый (этанол)
ректификованный
|
ГОСТ
Р 51652-2000 или ГОСТ
18300-87
|
|
Фосфор (V) оксид (фосфорный
ангидрид, пентоксид фосфора), хч
|
ТУ 6-09-4173-85
|
Примечание. Допускается использование реактивов с более высокой
квалификацией, не требующих дополнительной очистки растворителей.
|
Аппарат для встряхивания
|
ТУ 64-1-2851-78
|
|
Баня водяная
|
|
|
Бумажные фильтры высокой плотности,
обеззоленные (бумажные фильтры)
|
ТУ 2642-001-05015242-07
|
|
Бязь хлопчатобумажная белая
|
|
|
Воронка Бюхнера
|
ГОСТ
9147-80
|
|
Воронки конусные диаметром 40 - 45
мм
|
ГОСТ
25336-82
|
|
Груша резиновая
|
ТУ 9398-005-0576-908
|
|
Колба Бунзена
|
ГОСТ
25336-82
|
|
Колбы круглодонные на шлифе
вместимостью 150 см3
|
ГОСТ
9737-93
|
|
Линейка измерительная
|
ГОСТ
427-75
|
|
Мембраны микропористые капроновые,
размер пор 0,45 мкм
|
ТУ 9471-002-10471723-03
|
|
Набор для фильтрации растворителей
через мембрану
|
|
|
Насос водоструйный
|
ГОСТ
25336-82
|
|
Пинцет медицинский нержавеющий
|
ГОСТ
21241-89
|
|
Ректификационная колонна с числом
теоретических тарелок не менее 30
|
|
|
Ротационный вакуумный испаритель с
мембранным насосом, обеспечивающим вакуум до 10 мбар
|
|
|
Стаканы химические с носиком,
вместимостью 150 см3
|
ГОСТ
25336-82
|
|
Стекловата
|
|
|
Стеклянные емкости вместимостью
100 см3 с герметичной металлической крышкой
|
|
|
Стеклянные палочки
|
|
|
Установка для перегонки
растворителей
|
|
|
Фильтродержатель
|
|
|
Холодильник обратный
|
|
|
Хроматографическая колонка
стальная, длиной 250 мм, внутренним диаметром 4,6 мм, заполненная
обращенно-фазным сорбентом с привитыми монофункциональными полярными группами
С8, зернение 5 мкм
|
|
|
Шприц для ввода образцов для
жидкостного хроматографа вместимостью 50 - 100 мм3
|
|
Примечание. Допускается применение оборудования с аналогичными
или лучшими техническими характеристиками.
4.1. При выполнении измерений необходимо соблюдать требования
техники безопасности при работе с химическими реактивами по ГОСТ
12.1.007-76, требования по электробезопасности при работе с
электроустановками по ГОСТ
Р 12.1.019-09, а также требования, изложенные в технической документации на
жидкостный хроматограф.
4.2. Помещение должно соответствовать требованиям
пожаробезопасности по ГОСТ
12.1.004-91 и иметь средства пожаротушения по ГОСТ
12.4.009-83. Содержание вредных веществ в воздухе не должно превышать ПДК
(ОБУВ), установленных ГН
2.2.5.1313-03 и ГН
2.2.5.2308-07. Организация обучения работников безопасности труда - по ГОСТ
12.0.004-90.
К выполнению измерений допускают специалистов, имеющих
квалификацию не ниже лаборанта-исследователя, с опытом работы на жидкостном
хроматографе, освоивших данную методику и подтвердивших экспериментально
соответствие получаемых результатов нормативам контроля погрешности измерений
по п. 12.
К проведению пробоподготовки допускают оператора с
квалификацией «лаборант», имеющего опыт работы в химической лаборатории.
При выполнении измерений соблюдают следующие условия:
- процессы приготовления растворов и подготовки проб к
анализу проводят при температуре воздуха (20 ± 5) °С и относительной влажности
не более 80 %;
- выполнение измерений на жидкостном хроматографе проводят в
условиях, рекомендованных технической документацией к прибору.
Выполнению измерений предшествуют следующие операции:
очистка органических растворителей (при необходимости), подготовка подвижной
фазы для ВЭЖХ, кондиционирование хроматографической колонки, приготовление
растворов для градуировки и внесения, растворов для экстракции, установление
градуировочной характеристики, подготовка фильтров и салфеток для отбора проб,
отбор проб.
Ацетонитрил кипятят с обратным холодильником над пентоксидом
фосфора (на 1 дм3 ацетонитрила 20 г пентоксида фосфора) не менее 1
часа, после чего перегоняют, непосредственно перед употреблением ацетонитрил
повторно перегоняют над прокаленным карбонатом калия (на 1 дм3
ацетонитрила 10 г карбоната калия).
7.2.
Подготовка подвижной фазы для ВЭЖХ
В мерную колбу вместимостью 1000 см3 помещают 550
см3 бидистиллированной или деионизованной воды, добавляют 1 см3
фосфорной кислоты, 450 см3 ацетонитрила, перемешивают, фильтруют
через мембранный фильтр и дегазируют. Подвижную фазу хранят в темном месте (в
емкости из темного стекла) не более 14 дней.
Колонку промывают подвижной фазой (приготовленной по п. 7.2) при скорости
подачи растворителя 1,0 см3/мин до установления стабильной базовой
линии.
7.4.1. Исходный раствор
дифлуфензопира для градуировки (концентрация 100 мкг/см3). В
мерную колбу вместимостью 100 см3 помещают 0,0100 г дифлуфензопира, растворяют
в 50 см3 воды, доводят ацетонитрилом до метки, тщательно
перемешивают.
Раствор хранят в холодильнике при температуре 4 - 6 °С в
течение 10 дней.
Растворы № 1 - 5 готовят объемным методом путем
последовательного разбавления исходного раствора для градуировки.
7.4.2. Раствор № 1 дифлуфензопира для
градуировки и внесения (концентрация 10 мкг/см3). В мерную колбу
вместимостью 100 см3 помещают 10 см3 исходного раствора дифлуфензопира
с концентрацией 100 мкг/см3 (п. 7.4.1), доводят смесью ацетонитрил:вода (1:1, по
объему) до метки.
Градуировочный раствор № 1 хранят в холодильнике при
температуре 4 - 6 °С в течение 10 дней.
Этот раствор используют для приготовления проб с внесением
при оценке полноты извлечения действующего вещества методом «внесено-найдено»,
а также контроле качества результатов методом «добавок».
7.4.3. Рабочие растворы № 2 - 5
дифлуфензопира для градуировки (концентрация 0,1 - 1,0 мкг/см3).
В 4 мерные колбы вместимостью 100 см3 помещают по 1,0; 2,0; 5,0 и
10,0 см3 градуировочного раствора № 1 с концентрацией 10 мкг/см3
(п. 7.4.2), доводят до метки
подвижной фазой, приготовленной по п. 7.2, тщательно перемешивают, получают рабочие растворы №
2 - 5 с концентрацией дифлуфензопира 0,1; 0,2; 0,5 и 1,0 мкг/см3
соответственно.
Рабочие растворы для градуировки использовать в день
приготовления.
7.5.
Установление градуировочной характеристики
Градуировочную характеристику, выражающую зависимость
площади пика от концентрации дифлуфензопира в растворе, устанавливают методом
абсолютной калибровки по 4 растворам для градуировки № 2 - 5, приготовленным по
п. 7.4.3.
В инжектор хроматографа вводят по 20 мм3 каждого
градуировочного раствора и анализируют в условиях хроматографирования,
указанных ниже. Осуществляют не менее 5 параллельных измерений. Устанавливают
площади пиков дифлуфензопира, на основании которых строят градуировочную
зависимость.
Условия хроматографирования
Измерения выполняют при следующих режимных параметрах.
Жидкостный хроматограф с ультрафиолетовым детектором с
переменной длиной волны
Хроматографическая колонка стальная, длиной 250 мм,
внутренним диаметром 4,6 мм, заполненная обращенно-фазным сорбентом с привитыми
монофункциональными полярными группами С8, зернение 5 мкм
Рабочая длина волны: 240 или 290* нм
________
*
Хроматографирование пробы при 2 длинах волн увеличивает надежность
идентификации вещества
Температура колонки; комнатная
Подвижная фаза: ацетонитрил вода-ортофосфорная кислота
(45:55:0,1, по объему)
Скорость потока элюента: 1,0 см3/мин
Объем вводимой пробы: 20 мм3
Линейный диапазон детектирования: 2 - 20 нг.
Диаметр бумажного фильтра должен соответствовать внутреннему
диаметру фильтродержателя.
Фильтры последовательно по 3 раза промывают на воронке
Бюхнера этанолом, затем ацетонитрилом порциями 25 - 30 см3, сушат с
помощью разряжения, создаваемого водоструйным насосом, затем на воздухе при
комнатной температуре. До использования фильтры хранят в герметично закрытой
стеклянной таре.
7.7.1. Приготовление раствора натрия углекислого с
массовой долей 5 % (5 %-й раствор). Навеску (25 ± 0,1) г натрия углекислого
помещают в мерную колбу вместимостью 500 см3, растворяют в
деионизированной воде, доводят водой до метки, перемешивают.
7.7.2.
Подготовка салфеток для проведения смыва
Вырезают салфетки (лоскуты) из белой бязи размером
10×10 см, затем их последовательно обрабатывают 5 %-м раствором
углекислого натрия (при кипячении), водой до нейтральной реакции промывных вод,
2-кратно промывают этиловым спиртом, сушат на воздухе при комнатной
температуре. До использования салфетки хранят в герметично закрытой стеклянной
таре.
Отбор проб осуществляют в соответствии с требованиями ГОСТ
12.1.005-88 «ССБТ. Общие санитарно-гигиенические требования к воздуху
рабочей зоны» и Руководства Р
2.2.2006-05 (прилож. 9, обязательное) «Общие методические требования к
организации и проведению контроля содержания вредных веществ в воздухе рабочей
зоны», п. 2 «Контроль соответствия максимальным ПДК».
Воздух с объемным расходом 4 - 5 дм3/мин
аспирируют через бумажный фильтр, помещенный в фильтродержатель.
Для измерения концентрации вещества на уровне 0,02 мг/м3
необходимо отобрать 25 дм3 воздуха.
Срок хранения отобранных проб, помещенных в полиэтиленовые
пакеты, в холодильнике при температуре 4 - 6 °С - 30 дней.
Смывы проводят в конце работы или после выполнения отдельных
операций с открытых и закрытых спецодеждой или другими СИЗ участков тела (лоб,
лицо, шея, грудь, предплечье, голень, кисти рук, включая межпальцевые
промежутки).
До работы выбирают участок кожи, обрабатывают его для
удаления загрязнений, фиксируют площадь (не менее 200 см2). При
необходимости отбирают фоновые смывы.
Смыв выполняют способом обмыва фиксированного участка кожи
смесью этилового спирта с водой (8:2, по объему), помещая 20 см3 в
стеклянную емкость с металлической крышкой. Тканевой салфеткой, смоченной
растворителем, с помощью пинцета (индивидуально) обмывают этот участок сверху
вниз. Операцию повторяют дважды.
Срок хранения отобранных проб смывов, помещенных в
герметично закрытые емкости, в морозильной камере при температуре -18 °С - 30
дней.
Экспонированный фильтр переносят в химический стакан
вместимостью 150 см3, заливают 10 см3 смеси этанол-вода
(8:2, по объему), помещают на встряхиватель на 10 минут. Растворитель сливают,
фильтр еще дважды обрабатывают новыми порциями по 10 см3 указанной
смеси, выдерживая на встряхивателе по 10 минут.
Объединенный экстракт переносят (через воронку) в круглодонную
колбу, упаривают на ротационном вакуумном испарителе при температуре бани не
выше 40 °С почти досуха, оставшийся растворитель отдувают потоком теплого
воздуха. Остаток растворяют в 5 см3 подвижной фазы (подготовленной
по п. 7.2.),
тщательно перемешивают и анализируют при условиях хроматографирования,
указанных в п. 7.5.
Пробу смыва сливают (через воронку) в колбу для упаривания,
с помощью пинцета извлекают салфетку, помещают в конусную химическую воронку,
установленную в муфту колбы для упаривания, тщательно отжимают и промывают
смесью этанол-вода (8:2, по объему) дважды порциями по 10 см3,
предварительно ополаскивая смесью емкость, в которой находилась проба.
Объединенный раствор упаривают на ротационном вакуумном
испарителе при температуре бани не выше 40 °С почти досуха, оставшийся
растворитель отдувают потоком теплого воздуха. Остаток растворяют в 2 см3
подвижной фазы (подготовленной по п. 7.2.) и анализируют при условиях хроматографирования,
указанных в п. 7.5.
Пробу вводят в испаритель хроматографа не менее двух раз.
Устанавливают площадь пика дифлуфензопира, с помощью градуировочного графика
определяют концентрацию дифлуфензопира в хроматографируемом растворе.
Образцы, дающие пики большие, чем градуировочный раствор с
концентрацией 1,0 мкг/см3, разбавляют подвижной фазой (не более чем
в 50 раз).
Концентрацию вещества в пробе
воздуха (X), мг/м3, рассчитывают по формуле:
С - концентрация вещества в
хроматографируемом растворе, найденная по градуировочному графику в
соответствии с величиной площади хроматографического пика, мкг/см3;
W - объем экстракта, подготовленного для
хроматографирования, см3;
Vt - объем пробы воздуха, отобранный для анализа,
приведенный к стандартным условиям (давление 760 мм рт. ст., температура 20
°С), дм3.
Т - температура воздуха при
отборе проб (на входе в аспиратор), °С;
Р - атмосферное давление при отборе пробы, мм рт.
ст.;
u - расход воздуха при отборе
пробы, дм3/мин;
t - длительность отбора
пробы, мин:
R - коэффициент, равный 0,386 для воздуха рабочей
зоны.
Концентрацию вещества в пробе
смыва X, мкг/смыв, рассчитывают по формуле:
С - концентрация вещества в
хроматографируемом растворе, найденная по градуировочному графику в
соответствии с величиной площади хроматографического пика, мкг/см3;
W - объем экстракта, подготовленного для
хроматографирования, см3.
Примечание. Идентификация и расчет концентрации вещества в пробах
могут быть проведены с помощью компьютерной программы обработки
хроматографических данных, включенной в аналитическую систему.
Результат количественного анализа представляют в виде:
- результат анализа ![]() в мг/м3 или мкг/смыв (с
указанием площади смыва в см2), характеристика погрешности δ,
% (таблица), Р = 0,95 или
в мг/м3 или мкг/смыв (с
указанием площади смыва в см2), характеристика погрешности δ,
% (таблица), Р = 0,95 или ![]() ± Δ мг/м3 (мкг/смыв,
площадь смыва, см2), Р = 0,95, где
± Δ мг/м3 (мкг/смыв,
площадь смыва, см2), Р = 0,95, где
![]() - среднее арифметическое результатов
определений, мг/м3 (мкг/смыв);
- среднее арифметическое результатов
определений, мг/м3 (мкг/смыв);
Δ - граница абсолютной
погрешности, мг/м3 (мкг/смыв);
δ - граница
относительной погрешности методики (показатель точности по диапазону
концентраций, таблица), %,
Результат измерений должен иметь тот же десятичный разряд,
что и погрешность.
Если содержание вещества менее нижней границы диапазона
определяемых концентраций, результат анализа представляют в виде;
«содержание дифлуфензопира в пробе воздуха рабочей зоны -
менее 0,02 мг/м3; в пробе смыва - менее 0,2 мкг/смыв»*
* - 0,02 мг/м3; 0,2 мкг/смыв - пределы
обнаружения при отборе 25 дм3 воздуха рабочей зоны; в пробе смыва
(фиксированная площадь смыва, 200 см2) соответственно.
12.
Контроль качества результатов измерений
Оперативный контроль погрешности и воспроизводимости
измерений осуществляется в соответствии с ГОСТ Р ИСО 5725-(1
- 6)-02
«Точность (правильность и прецизионность) методов и результатов измерений».
![]() - среднее значение массовой
концентрации анализируемого компонента в пробе (мг/м3, мкг/смыв).
- среднее значение массовой
концентрации анализируемого компонента в пробе (мг/м3, мкг/смыв).
12.1. Контроль стабильности градуировочной характеристики
проводят в начале и по окончании каждой серии анализов.
При контроле стабильности градуировочной характеристики
проводят измерения не менее трех образцов растворов для градуировки, содержание
дифлуфензопира в которых должно охватывать весь диапазон концентраций от 0,1 до
1,0 мкг/см3.
Градуировочная характеристика
считается стабильной, если для каждого из используемого для контроля
градуировочного раствора сохраняется соотношение;
X - концентрация
дифлуфензопира в пробе при контрольном измерении, мкг/см3;
С - известная концентрация градуировочного раствора
дифлуфензопира, взятая для контроля стабильности градуировочной характеристики,
мкг/см3;
В - норматив контроля погрешности градуировочной
характеристики, % (В = 10 % при Р = 0,95).
Если величина расхождения (А) превышает 10 %, делают
вывод о невозможности применения градуировочной характеристики для дальнейших
измерений. В этом случае выясняют и устраняют причины нестабильности
градуировочной характеристики и повторяют контроль ее стабильности с использованием
других градуировочных растворов дифлуфензопира, предусмотренных МВИ. При
повторном обнаружении нестабильности градуировочной характеристики
устанавливают ее заново согласно п. 7.5.
Стабильность результатов измерений контролируют перед
проведением измерений, анализируя один из градуировочных растворов.
12.2. Плановый внутрилабораторный оперативный контроль
процедуры выполнения анализа проводится методом добавок.
Образцами дам контроля являются реальные пробы воздушной
среды и смывов с кожных покровов. Объем отобранных для контроля процедуры
выполнения анализа проб воздуха и смывов с кожи должен соответствовать
удвоенному объему, необходимому для проведения анализа по методике,
фиксированная площадь смыва должна быть увеличена в 2 раза. После отбора проб
экстракт с фильтра, а также пробу смыва делят на две равные части, первую из
которых анализируют в точном соответствии с прописью методики и получают
результат анализа исходной рабочей пробы - X. Во вторую часть делают
добавку анализируемого компонента (величина добавки Сд должна
соответствовать 50 - 150 % от содержания компонента в пробе, общая концентрация
не должна превышать верхнюю границу диапазона измерения) и анализируют в точном
соответствии с прописью методики, получая результат анализа рабочей пробы с
добавкой - Xʹ. Результаты анализа исходной рабочей пробы (X)
и рабочей пробы с добавкой (X) получают в условиях повторяемости (один
аналитик, использование одного набора мерной посуды, одной партии реактивов и
т.д.).
Величина добавки Сд
должна удовлетворять условию:
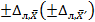 - характеристика погрешности
(абсолютная погрешность) результатов анализа, соответствующая содержанию
компонента в испытуемом образце (расчетному значению содержания компонента в
образце с добавкой), мг/м3, мкг/смыв.
- характеристика погрешности
(абсолютная погрешность) результатов анализа, соответствующая содержанию
компонента в испытуемом образце (расчетному значению содержания компонента в
образце с добавкой), мг/м3, мкг/смыв.
Допустимо характеристику
погрешности результатов анализа при внедрении методики в лаборатории
устанавливать на основе выражения Δл = ±0,84Δ с последующим
уточнением по мере накопления информации, где Δ - граница абсолютной
погрешности, мг/м3, мкг/смыв;
δ - граница
относительной погрешности методики (показатель точности в соответствии с
диапазоном концентраций, таблица), %.
Контроль проводят путем сравнения результата контрольной
процедуры Кк с нормативом контроля К.
Результат контрольной процедуры Ккрассчитывают по формуле:
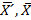 , Сд - среднее
значение массовой концентрации анализируемого компонента в образце с добавкой,
испытуемом образце, концентрация добавки соответственно (мг/м3,
мкг/смыв).
, Сд - среднее
значение массовой концентрации анализируемого компонента в образце с добавкой,
испытуемом образце, концентрация добавки соответственно (мг/м3,
мкг/смыв).
Норматив оперативного контроля
точности К рассчитывают по формуле:
Проводят сопоставление результата
контрольной процедуры (Кк) с нормативом контроля (К).
Если результат контрольной
процедуры удовлетворяет условию
процедуру анализа
признают удовлетворительной.
При невыполнении условия (1)
процедуру контроля повторяют. При повторном невыполнении условия (1) выясняют причины, приводящие к неудовлетворительным
результатам, и принимают меры по их устранению.
12.3. Проверка приемлемости результатов измерений,
полученных в условиях воспроизводимости.
Расхождение между результатами
измерений, выполненных в условиях воспроизводимости (разное время, разные
операторы, разные лаборатории), не должно превышать предела воспроизводимости (R):
R =
0,15⋅![]() ; (воздух рабочей зоны)
; (воздух рабочей зоны)
R = 0,24⋅![]() ; (смывы с кожи)
; (смывы с кожи)
![]() = ½(Х1 + Х2),
где Х1, Х2 - результаты измерений в
условиях воспроизводимости (разное время, разные операторы, разные
лаборатории), мг/м3, мкг/смыв.
= ½(Х1 + Х2),
где Х1, Х2 - результаты измерений в
условиях воспроизводимости (разное время, разные операторы, разные
лаборатории), мг/м3, мкг/смыв.
R - предел воспроизводимости (таблица), мг/м3, мкг/смыв.
Если выполняется условие (2),
то воспроизводимость измерений считается удовлетворительной.
При превышении норматива контроля воспроизводимости
эксперимент повторяют, при повторном превышении указанного норматива выясняют
причины и по возможности их устраняют.
Новости
Библиотека
Soft по ОТ и ПБ
Консультации
Агрегатор
Услуги
Форум
Золотой фонд
ССОТ
CHAT-OT


.webp)