| ФЕДЕРАЛЬНОЕ АГЕНТСТВО
ПО ТЕХНИЧЕСКОМУ РЕГУЛИРОВАНИЮ И МЕТРОЛОГИИ |
| 
| НАЦИОНАЛЬНЫЙ
СТАНДАРТ
РОССИЙСКОЙ
ФЕДЕРАЦИИ | ГОСТ Р ИСО
11133-1-
2008 |
МИКРОБИОЛОГИЯ ПИЩЕВЫХ ПРОДУКТОВ И КОРМОВ ДЛЯ ЖИВОТНЫХ
Руководящие указания по приготовлению и производству культуральныхсред
Часть 1
Общие руководящие указания по обеспечению качества приготовлениякультуральных сред в лаборатории
ISO 11133-1:2000
Microbiology of food and animal feeding stuffs - Guidelines on preparation andproduction of culture media - Part 1: General guidelines on quality assurancefor the preparation of culture media in the laboratory
(IDT)
| 
| Москва Стандартинформ 2009 |
Цели и принципы стандартизации вРоссийской Федерации установлены Федеральным законом от 27 декабря 2002 г. № 184-ФЗ «О техническомрегулировании», а правила применения национальных стандартов РоссийскойФедерации - ГОСТ Р1.0-2004 «Стандартизация в Российской Федерации. Основные положения»
Сведения о стандарте
1 ПОДГОТОВЛЕН Государственным учреждением«Научно-исследовательский институт эпидемиологии и микробиологии именипочетного академика Н.Ф. Гамалеи» Российской академии медицинских наук наоснове русской версии стандарта, указанного в пункте 4
2 ВНЕСЕН Техническим комитетом постандартизации ТК 335 «Методы испытаний агропромышленной продукции набезопасность»
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ ПриказомФедерального агентства по техническому регулированию и метрологии от 18 декабря2008 г. № 478-ст
4 Настоящий стандарт идентичен международномустандарту ИСО 11133-1:2000 «Микробиология пищевых продуктов и кормов дляживотных. Руководящие указания по приготовлению и производству культуральныхсред. Часть 1. Общие руководящие указания по обеспечению качества приготовления культуральных сред в лаборатории» (ISO11133-1:2000 «Microbiology of food and animal feeding stuffs - Guidelines onpreparation and production of culture media - Part 1: General guidelines onquality assurance for the preparation of culture media in the laboratory»)
5 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему стандартупубликуется в ежегодно издаваемом информационном указателе «Национальныестандарты», а текст изменений и поправок - в ежемесячно издаваемыхинформационных указателях «Национальные стандарты». В случае пересмотра (замены)или отмены настоящего стандарта соответствующее уведомление будет опубликованов ежемесячно издаваемом информационном указателе «Национальные стандарты».Соответствующая информация, уведомление и тексты размещаются также винформационной системе общего пользования - на официальном сайте Федеральногоагентства по техническому регулированию и метрологии в сети Интернет
Содержание
Введение
В микробиологической лабораториибольшинство испытаний и процедур зависит от качества культуральных сред,обеспечивающих получение воспроизводимых результатов. Культуральные средыиспользуют во всех традиционных методах выращивания микроорганизмов, а такжедля множества альтернативных задач. В продаже имеется широкий ассортимент готовыхкультуральных сред - обезвоженных концентратов. Еще больше составовкультуральных сред, предназначенных конкретно для выращивания микроорганизмов,описано в литературе. Кроме того, в лабораториях, занятых микробиологическимиисследованиями пищевых продуктов, основными целями является поддержание,оживление, выращивание, обнаружение и/или подсчет самых разнообразныхмикроорганизмов. Требования к среде являются специфичными как к пробе, так и кискомым микроорганизмам. Поэтому культуральные среды, удовлетворяющиеустановленным или минимальным критериям эффективности, являются необходимымусловием надежных результатов любого микробиологического исследования. Чтобыубедиться в приемлемости каждой партии питательной среды, пригодности среды длярешения поставленной задачи и возможности получения на данной средевоспроизводимых непротиворечивых результатов, необходимо выполнить достаточныйобъем испытаний.
Эти три критерия являются важнойчастью внутреннего контроля качества и при наличии соответствующей документациипозволяют осуществлять эффективный контроль культуральных сред, чтобыобеспечивать получение точных и объективных результатов.
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
МИКРОБИОЛОГИЯ ПИЩЕВЫХПРОДУКТОВ И КОРМОВ ДЛЯ ЖИВОТНЫХ
Руководящие указания поприготовлению и производству культуральных сред
Часть 1
Общие руководящие указанияпо обеспечению качества приготовления культуральных сред в лаборатории
Microbiology of food and animal feeding stuffs.Guidelines on preparation and production of culture media. Part 1. Generalguidelines on quality assurance for the preparation of culture media in thelaboratory
Дата введения - 2010-01-01
В настоящем стандартепредоставлена общая терминология, связанная с обеспечением качества приготовлениякультуральных сред, и установлены минимальные требования, которые следуетиспользовать для микробиологического анализа продуктов, предназначенных дляпотребления в пищу и корма для животных.
Эти требования применимы к тремкатегориям культуральных сред, используемых в лабораториях, которые готовяти/или используют культуральные среды для выполнения микробиологическихисследований:
- коммерческим средам, готовым киспользованию;
- средам, приготовленным изимеющихся в продаже сухих (обезвоженных) ингредиентов (это или среды,включающие все необходимые для рецептуры ингредиенты, например агаризованнаясреда для подсчета колоний (plate count agar - РСА) или основные среды, к которым добавляют отдельные ингредиенты,например агаровая среда Байд-Паркера (Baid-Parkeragar));
- средам, приготовленным отиндивидуальных ингредиентов.
В настоящем стандартеиспользованы нормативные ссылки на следующие стандарты:
ЕН 1659:1996 Системы длядиагностики in vitro. Культуральныесреды для микробиологических целей. Термины и определения.
ЕН 12322:1999 Средствамедицинские для диагностики in vitro. Культуральныесреды для микробиологических целей. Критерии эффективности культуральных сред.
ИСО 8402:1994 Управлениекачеством и обеспечение качества. Словарь.1)
1) Стандарт в настоящее время пересматривается и будетобъединен с ИСО 9000-1:1994 с целью создания ИСО 9000:2000 «Системы менеджментакачества. Основные положения и словарь».
В этом разделе приводятся общие определения, связанные с обеспечениемкачества, и различные термины, касающиеся питательных сред и выращиваниякультур. Стандарты, приведенные в скобках, указывают на то, что данный текстидентичен тексту из этих стандартов.
| 3.2.1 обеспечение качества: Все виды плановой и систематической деятельности, осуществленные в пределах системы качества и считающиеся необходимыми для обеспечения адекватных условий, которые обеспечивают требования по качеству ИСО [8402] |
| |
| 3.2.2 контроль качества: Операционные методы и деятельность персонала для выполнения требований по качеству [ИСО 8402] |
| |
| 3.2.3 внутренний контроль качества: Непрерывная программа контроля работы лаборатории, подготовленная самой лабораторией или для нее основанная на анализе контроля качества с корректировкой исполнения, если это необходимо. [ИСО 8402] |
3.2.4 партиякультуральных сред: Полностью прослеживаемая единица среды, относящаяся к определенномуколичеству концентрата, полуфабриката или конечного продукта, котораяизготовлена в соответствии с требованиями производства (контроль в процессеприготовления) и проверена на соответствие установленным требованиям качества,была произведена в течение определенного периода производства и которойприсвоен один номер партии.
3.2.5 эффективностькультуральных сред: Реакция питательной среды при посеве на нее контрольныхорганизмов при определенных условиях.
| 3.3.1 культуральная среда: Перечень ингредиентов, в жидкой, полужидкой или в твердой формах, которые содержат натуральные и/или синтетические компоненты для того, чтобы поддерживать размножение или сохранять жизнеспособность микроорганизмов. Примечание - При использовании культуральных сред, состоящих из ингредиентов со сложными словами, термин часто сокращают и обозначают как «среда» (например, среда обогащения). [ЕН 1659] |
| 3.3.2 Классификация культуральных сред в соответствии с составом |
| 3.3.2.1 культуральная среда с химически определенным составом: Питательная среда, состоящая только из химически определенных ингредиентов (то есть, с известной молекулярной структурой и степенью чистоты). [ЕН 1659] |
| 3.3.2.2 культуральная среда с не полностью охарактеризованным химическим составом: Культуральная среда, состоящая полностью или частично из природных материалов, обработанных или неизмененных, химический состав которых определен не полностью. Примечание - Для различных, химически неопределенных компонентов, используемых в культуральных средах, приведен перечень в приложении А. 3.3.3 Культуральные среды, классифицируемые по консистенции |
| 3.3.3.1 жидкая культуральная среда: Культуральная среда, состоящая из водного раствора одного или более компонентов (например, пептонная вода, питательный бульон). Примечания 1 В некоторых случаях к жидкой культуральной среде добавлены твердые частицы. 2 Жидкие культуральные среды в пробирках, флаконах или колбах обычно называют «бульон» [ЕН 1659] |
3.3.3.2 плотная культуральная среда иполужидкая культуральная среда: Плотная культуральная среда, содержащаязатвердевающие материалы (например, агар-агар, желатин и т.д.,), в различныхконцентрациях.
Примечания
1 Из-за международного использования культуральные среды сзатвердителем агар-агаром часто обозначают сокращенно термином «агар» длятвердых культуральных сред, например «агар для подсчета колоний на чашкахПетри».
2 Твердыекультуральные среды, разлитые в чашки Петри, обычно называют «чашка». Твердыекультуральные среды, разлитые в пробирки, которые размещают в наклонномположении при затвердевании среды часто называют «косяками» или «скошеннымагаром».
[ЕН 1659]
3.3.4 Классификация культуральных сред по назначению
| 3.3.4.1 транспортная среда: Культуральная среда, предназначенная для сохранения и поддержания жизнеспособности микроорганизмов с момента отбора образца до начала ее анализа в лаборатории. Примечание - Транспортные среды обычно содержат вещества, которые не допускают размножения микроорганизмов, но гарантируют их сохранение (например, транспортная среда Стюарта или среда Эймса). [ЕН 1659] |
| |
| 3.3.4.2 среда для сохранения микроорганизмов: Культуральная среда, предназначенная для сохранения и поддержания жизнеспособности микроорганизмов в течение продолжительного периода, чтобы защищать их против неблагоприятных влияний, которые могут происходить в течение долгосрочного хранения и позволять восстанавливать рост микроорганизма после этого периода (например, яичная среда Дорсе (Dorse). [ЕН 1659] |
| |
| 3.3.4.3 среда восстановления: Культуральная среда, позволяющая находящимся в состоянии стресса и ослабленным микроорганизмам восстанавливать способность для нормального роста без обязательного условия их размножения. [ЕН 1659] |
| |
| 3.3.4.4 среда обогащения: Преимущественно жидкая культуральная среда, которая благодаря ее составу обеспечивает особенно благоприятные условия для размножения микроорганизмов. [ЕН 1659] |
| 3.3.4.4.1 селективная среда обогащения: Среда обогащения, которая поддерживает размножение определенных микроорганизмов, частично или полностью подавляя рост других микроорганизмов (например, среда Раппапорта-Василиадиса (Rappaport-Vassiliadis). 3.3.4.4.2 неселективная среда обогащения: Среда обогащения, которая поддерживает рост большинства микроорганизмов (например, питательный «бульон»). 3.3.4.5 среда для выделения отдельных (изолированных) колоний: Плотная или полужидкая культуральная среда, которая поддерживает рост микроорганизмов. |
| 3.3.4.5.1 селективная среда для выделения отдельных (изолированных) колоний: Селективная среда, которая поддерживает рост определенных микроорганизмов, при отсутствии роста других микроорганизмов (например, агар PALCAM, агар MacConkey (МакКонки). [ЕН 1659] |
| |
| 3.3.4.5.2 неселективная среда для выделения отдельных колоний: Среда выделения, которая не предназначена для избирательного подавления роста микроорганизмов (например, питательный агар). [ЕН 1659] |
| |
| 3.3.4.6 дифференциальная (культуральная) среда: Культуральная среда, с помощью которой определяют одну или более физиологических/биохимических характеристик микроорганизмов для их идентификации (например, среда с мочевиной, агар Клиглера (Kligler). Примечание - Дифференциальные среды, которые можно использовать в качестве разделительных сред, называют разделительными/дифференциальными средами (например, агар на основе дезоксихолат-лизин-ксилозы (XLD). [ЕН 1659] |
| |
| 3.3.4.7 среда для идентификации: Культуральная среда, предназначенная для выявления определенной реакции идентификации, которая далее не требует дальнейшего подтверждения исследования. Примечание - Среды для идентификации, которые могут использоваться в качестве сред для выделения, относятся к средам идентификации/выделения. [ЕН 1659] |
| 3.3.4.8 культуральные среды, имеющие многоцелевое использование: Определенные культуральные среды могут принадлежать к нескольким категориям, например кровяной агар является средой восстановления согласно 3.3.4.3, средой выделения согласно 3.3.4.5 и дифференциальной средой согласно 3.3.4.6, используемой для обнаружения гемолиза. 3.3.5 Культуральные среды, классифицируемые в соответствии с методом приготовления 3.3.5.1 среда, готовая к использованию: Культуральная среда, находящаяся в контейнерах в готовой к использованию форме (например, чашки Петри или пробирки, или другие контейнеры) 3.3.5.2 культуральная среда, приготовленная из коммерческих сухих (обезвоженных) реагентов: Культуральная среда в сухой форме, которая не готова к немедленному использованию (например, порошки, гранулы, лиофилированные изделия). Повторная гидратация позволяет получить один из двух видов сред: - среда, полностью готовая к использованию; - среда, к которой добавляют неустойчивые компоненты непосредственно перед использованием. 3.4 Термины, используемые для характеристики контрольных микроорганизмов 3.4.1 контрольные микроорганизмы: Тест-микроорганизмы обычно используют для контроля качества и испытания эффективности культуральных сред. |
| 3.4.2 контрольный (эталонный) штамм: Микроорганизм, для которого определен род и вид. Микроорганизм внесен в каталог и описан согласно его характеристикам. Предпочтительно, чтобы было установлено его происхождение. [ЕН 12322] |
| |
| 3.4.3 контрольные (эталонные) культуры: Набор отдельных идентичных культур, полученных в лаборатории посредством получения от одного пересева из контрольного штамма либо имеющегося в лаборатории или полученного от поставщика. [ЕН 12322] |
3.4.4 рабочаякультура: Первичная субкультура, полученная от контрольного посеваконтрольной культуры (см. 3.4.3).
4.1.1Документация, предоставляемая изготовителем
Документация, предоставляемаяизготовителем, включает следующее:
- наименование среды, отдельныхингредиентов и всех добавок, включая их товарные коды;
- код партии;
- значение рН среды передприменением;
- информацию о хранении и датуистечения срока годности;
- оценку эффективности и используемыйтест-(микро)организм;
- техническую спецификацию;
- свидетельство о контролекачества;
- данные по опасности/защите(при необходимости).
4.1.2 Контрольная карталаборатории
Контрольная карта лабораториипосле получения среды включает следующую информацию:
- наименование среды и кодпартии;
- дату получения;
- дату истечения срока годности;
- состояние и целостностьупаковки
4.2.1 Общие положения
Во всех случаях следуютинструкциям изготовителя, где имеются данные об условиях хранения, срокеистечения и времени использования.
4.2.2 Управление качеством иконтроль качества сухих (обезвоженных) сред и добавок
Среды поставляют в обезвоженных(сухих) в виде порошка или гранул, в герметично упакованных контейнерах, адобавки различных селективных или диагностических реагентов в лиофилизированнойили жидкой формах.
Приобретение сред следуетпланировать таким образом, чтобы обеспечивать регулярный поток (т.е. первымполучено - первым использовано).
Для поддержания эффективногоучета необходимые проверки должны включать в себя:
- проверку герметичности;
- проверку даты первого вскрытиясред и добавок;
- визуальную оценку содержимогооткрытых контейнеров.
После открытия нового контейнерана качество среды может повлиять окружающая среда, в которой хранят открытыеконтейнеры со средами и добавками. Потеря качества сухих (обезвоженных) средпроявляется в изменении текучести порошка, гомогенности, образовании комков,изменении цвета и т.д. Любую сухую (обезвоженную) среду, которая стала влажнойили проявляет очевидные изменения физических свойств, следует исключать издальнейшей работы.
4.2.3 Коммерческие среды,готовые к использованию
В отношении условий хранения,времени использования сред и даты истечения срока годности необходимо соблюдатьинструкцию изготовителя.
4.2.4 Среды, приготовленныеиз имеющихся в продаже доступных сухих (обезвоженных) ингредиентов и основныхиндивидуальных компонентов
Срок годности сред,приготовленных из имеющихся в продаже доступных сухих (обезвоженных)ингредиентов и основных индивидуальных компонентов, различен. Пользовательвправе установить общие сроки хранения приготовленных сред. Специальныемеждународные или национальные стандарты могут предписывать конкретные условияи срок годности.
Стерилизованные среды, разлитыев чашки, пробирки или флаконы и реагенты, которые не используются немедленно,должны быть защищены от света и высыхания.
Если дата истечения срокагодности не была установлена или не указана в международном стандарте, среды, ккоторым конечные компоненты добавляют непосредственно перед использованием,следует хранить в холодильнике не более 3 мес или при комнатной температуре неболее одного месяца в условиях, не допускающих изменения их состава. Однакорекомендуется, чтобы среды, к которым добавляют селективные добавки,использовать в день их приготовления. Плотные среды, содержащие химическиактивные и/или неустойчивые вещества, следует хранить в таре, в которойосуществляют их плавление.
Следует наблюдать за любымизменением цвета, признаками появления пыли, обезвоживания или микробногороста. Партии сред, показывающие такие изменения, не следует использовать.
До использования или переднагреванием рекомендуется доводить среды до температуры окружающей среды.
4.3.1 Общие положения
Аккуратное приготовление сред -один из фундаментальных принципов в микробиологической экспертизе, и этомунеобходимо уделять особое внимание.
Необходимо следовать хорошейлабораторной практике и инструкциям изготовителя, касающимся работы с сухими(обезвоженными) средами и другими компонентами, входящими в их состав, особенносодержащими опасные материалы, такие как соли желчных кислот или другиеселективные компоненты.
Когда среды приготовляют изсухих (обезвоженных) коммерческих составов, необходимо точно выполнятьинструкции изготовителя. Документ (см. 4.1.1) дополнительнодолжен содержать информацию о порядке приготовления сред.
Для сред, приготовляемых изотдельных компонентов, необходимо строго соблюдать все операции,предусмотренные в инструкции изготовителя. Кроме того, до начала приготовлениясред следует проверить полную идентичность (то есть код и номер партии) всех используемыхкомпонентов.
4.3.2 Вода
Используемая вода должна бытьдистиллированной или равноценной по качеству, то есть освобожденной от веществ,которые могут ингибировать или влиять на рост микроорганизмов при контрольныхисследованиях. Если дистиллированную воду приготавливают из хлорированной воды,хлор необходимо нейтрализовать перед дистилляцией.
Дистиллированную воду следуетхранить в контейнерах, изготовленных преимущественно из инертных материалов(например, нейтральное стекло, полиэтилен и т.д.), которые должны бытьсвободными от ингибирующих рост микроорганизмов, веществ до их начальногоиспользования.
Примечание - В некоторыхслучаях может быть необходимо использовать свежеприготовленную воду, свободнуюот растворенной в ней двуокиси углерода.
Дистиллированная водахорошего качества должна иметь удельное сопротивление, по меньшей мере, 300000Ом×см.
Предупреждение! Вода, пропущенная через ионообменные устройства(деионизированная), может быть обсеменена высоким количеством микроорганизмов;желательно такую воду не использовать без подтверждения низкого содержания вней микроорганизмов. За консультацией о выборе лучшего метода минимизациизаражения микроорганизмами можно обратиться к изготовителю. Значительнозагрязненная микроорганизмами деионизированная вода, которая была стерилизованафильтрованием, может содержать достаточно веществ, подавляющих рост некоторыхмикроорганизмов.
4.3.3 Взвешивание иперегидратация (растворение)
Тщательно взвешиваютсоответствующее количество сухой (обезвоженной) среды при соблюдении мерпредосторожности, чтобы не вдохнуть порошок, особенно для среды, содержащейядовитые вещества. Для растворения постепенно добавляют требуемое количествоводы, избегая образования комков.
4.3.4 Растворение и дисперсия
Сухие (обезвоженные) средынуждаются в быстрой дисперсии путем постоянного перемешивания с нагреванием,если необходимо, для растворения. Средам, содержащим агар, нужно дать несколькоминут для впитывания воды с перемешиванием до нагревания. Для сред,приготовляемых из отдельных компонентов, каждый компонент необходимо добавлятьотдельно и полностью растворять, прежде чем окончательно довести до конечногообъема.
4.3.5 Измерение и получениенужной рН
рН измеряют, используя рН-метр,и получают необходимую рН, если среду приготовляют из отдельных компонентов влаборатории таким образом, чтобы после стерилизации и охлаждения до температуры25 °С среда имела требуемое значение рН + 0,2 единицы рН, если нет другихуказаний. Нужное значение рН получают с помощью гидроокиси натрия (NaOH) концентрацией приблизительно 40 г/л(приблизительно 1 мол/л) или соляной кислотой (HCl) приблизительно 36,5 г/л (приблизительно 1мол/л).
Примечание - Имеющиеся впродаже готовые среды могут показывать существенные изменения рН до и послеавтоклавирования. Однако если используют дистиллированную или деионизированнуюводу хорошего качества, то получение нужной рН до аквтоклавирования нетребуется.
4.3.6 Разливка
Среду разливают всоответствующие контейнеры, имеющие объем в 1,2-3 раза, превосходящий объемсреды.
4.3.7 Стерилизация
4.3.7.1 Общие положения
Стерилизацию культуральных среди реактивов можно выполнять, используя стерилизацию горячим паром (см. 4.3.7.2) илифильтрацией (см. 4.3.7.3).
Определенные среды не нуждаютсяв стерилизации автоклавированием и их допускается использовать после кипячения.Например, среды для выращивания Enterobacteriaceae, содержащие брилиантовый зеленый, особенночувствительны к нагреванию и действию и после кипячения должны быть быстроохлаждены и защищены от сильного света. Также некоторые реактивы допускаетсяиспользовать без стерилизации (см. соответствующий международный стандарт илиинструкции изготовителя).
4.3.7.2Стерилизация горячим паром
Стерилизацию горячим паромосуществляют в автоклаве или в специальном аппарате для приготовлениякультуральных сред. Обычно автоклавирование проводят в течение 15 мин притемпературе 121 °С. Для объемов более чем 1000 см3, циклстерилизации адаптируют соответствующим образом. Во всех случаях следуют всоответствии с инструкциями, данными в стандарте, и инструкциям изготовителей.Работу автоклава контролируют с помощью показаний термопар и индикаторныхполосок при типичных условиях, чтобы гарантировать достижение желаемоготемпературного профиля.
Примечание - Можетпроисходить перегревание, когда в автоклаве стерилизуются большие объемы сред(1000 см3).
Контроль эффективностистерилизации является существенным в приготовлении культуральных сред.
После нагревания следуетохлаждать среды способом, предотвращающим выкипание. Это особенно важно длячувствительных сред, например, предназначенных для Enterobacteriaceae, и сред, автоклавируемых в больших объемах.
4.3.7.3Стерилизация фильтрацией
Стерилизация фильтрацией можетбыть выполнена в вакуумных или герметичных условиях. Используют мембраны ифильтровальные элементы с диаметром пор 0,22 мкм. Они должны быть стерилизованыв автоклаве. При приобретении элементов фильтра и мембран в стерильномсостоянии при их использовании следуют инструкциям изготовителя. Стерилизуютразличные части аппарата фильтрации в собранном или разобранном состоянии вавтоклаве в течение 15 мин при температуре 121 °С. Если необходимо, послеавтоклавирования сборку в стерильных условиях осуществляют в ламинарном шкафу сочищенным потоком воздуха.
Примечание - На некоторыхфильтровальных мембранах могут задерживаться белки (такие как антибиотики).Чтобы получать необходимую концентрацию, пользователь должен использоватьпредварительно увлажненный фильтр.
4.3.7.4 Мониторинг (слежение)
После автоклавирования,кипячения или фильтрации во всех средах проверяют значение рН, цвет,стерильность и консистенцию.
4.3.8 Приготовление добавок
Коммерческие добавки, содержащиетоксические агенты, особенно антибиотики, следует приготовлять с осторожностью,избегая распыления порошка, который может вызывать аллергические или другиереакции у персонала лаборатории. При приготовлении добавок необходимо соблюдатьтехнику безопасности и следовать инструкциям изготовителя. Не допускаетсяиспользовать добавки с просроченным сроком годности. Например, для рабочихрастворов антибиотика срок годности истекает в тот же самый день. Приопределенных обстоятельствах растворы антибиотика допускается хранить взамороженном состоянии в соответствующих объемах (аликвотах). Не допускается ихповторное замораживание после оттаивания. Потенциальная потеря активностивследствие замораживания должна быть обсуждена с изготовителем или определенапользователем.
4.4.1 Плавление агаровыхкультуральных сред
Плавление культуральной средыосуществляют, поместив ее в кипящую водяную баню или любым другим способом,дающим идентичные результаты (например, в автоклаве с проходящим потоком пара).Среды, которые ранее были автоклавированы, повторно нагревают в течениеминимального времени, чтобы сохранять качество среды. Следует избегатьперегрева и удалять среду из водяной бани, когда она расплавилась. Охлаждаютрасплавленную среду до температуры (47 ± 2) °С в водяной бане с контролем температуры втечение времени до ее использования. Время, необходимое для достижениятемпературы 47 °С, зависит от вида среды, объема и количества флаконов вводяной бане. Расплавленную среду следует использовать, как можно скорее, повозможности, сразу, но не более чем через 4 ч.
4.4.2 Деаэрация культуральныхсред
Если необходимо, доиспользования нагревают культуральную среду в кипящей воде или в потоке пара втечение 15 мин, приоткрыв крышку или пробку; после нагревания крышки или пробкиплотно закрывают и быстро охлаждают до необходимой температуры.
4.4.3 Введение дополнительныхдобавок
Термолабильные (неустойчивые кнагреванию) добавки следует добавлять в среду после ее охлаждения до (47 ± 2)°С. Стерильная добавка перед добавлением к агаровой среде должна быть доведенадо комнатной температуры. Холодные жидкости могут привести к образованию геляиз агара или сформировать прозрачные хлопья. Все добавки добавляют в средуосторожно и перемешивают до полного растворения, затем наливают в конечныеконтейнеры, по возможности, максимально быстро насколько это возможно.
4.4.4 Приготовление ихранение сред в чашках Петри
Разливают агаровую среду в чашкиПетри, чтобы получить слой толщиной не менее 2 мм (например, для чашекдиаметром 90 мм обычно требуется 15 см3 среды). Чтобы дать агаровойсреде охладиться и застыть, чашки Петри, закрытые крышками, помещают напрохладную, горизонтальную поверхность.
Примечание - В течениеинкубации будет происходить потеря влажности агаровой среды. Потеря больше, чем15 % водного содержимого, может в некоторых случаях неблагоприятно влиять нарост микроорганизмов. Факторы, влияющие на потерю воды, включают в себя составсреды, количество среды в чашках, тип термостата (с вентиляцией или без нее),влажность атмосферы в термостате, расположение и количество чашек в термостатеи температуру инкубации.
Разлитую и застывшую средуиспользуют немедленно или хранят при условиях, предотвращающих изменение еесостава, то есть в темноте и/или в холодильнике при температуре 4 °С - 12 °С взакрытых контейнерах в течение одной недели или в соответствии с указаниямиизготовителя, или указаниями определенного стандарта на конкретный видисследования. Чашки маркируют, указывая дату приготовления и/или дату истечениясрока годности и идентификации. Допускается использовать альтернативные системыкодирования, удовлетворяющие этим требованиям.
Срок годности чашек с разлитойагаровой средой можно увеличить, если хранить их в герметично закрытыхполиэтиленовых пакетах. Чтобы избежать появления конденсата, чашки необходимоохладить перед помещением в пакеты. Не допускается подсушивание поверхностиагаровых чашек перед хранением в охлажденном состоянии.
До инокуляции твердойпитательной среды на поверхность плотной питательной среды чашки подсушивают,предпочтительно с удаленными крышками и с поверхностью агара, повернутой вниз,в сушильном шкафе при температуре от 25 °С до 50 °С или в ламинарном боксе, покас поверхности агаровой среды не исчезнут капли влаги. Нельзя пересушиватьчашки. Чашки с готовой к использованию агаризованной средой, приобретенной впродаже, должны храниться и использоваться согласно инструкции изготовителя.
4.4.5 Инкубация в термостате
Чашки рекомендуется ставить встопки не более чем по 6 шт. в высоту. Следует оставлять пространство дляциркуляции воздушного потока, чтобы среда быстро пришла в равновесие стемпературой инкубации в термостате настолько, насколько это возможно. Для жидкихсред время для достижения температуры инкубации зависит от ряда факторов,например объема, размещения, типов контейнеров, типов термостата. В случаевыращивания в анаэробных условиях может оказаться необходимым сложить чашки встопки не менее шести чашек в стопке.
Контаминированные инеиспользованные культуральные среды следует удалять безопасным способом всоответствии с национальными правилами.
Лабораторное тестирование должновключать в себя, как минимум:
- показатель РН, измеренный притемпературе 20 °С и 25 °С;
- количество заполнения и/илитолщину слоя;
- цвет;
- прозрачность/присутствиеоптических артефактов;
- стабильность/консистенцию/влажностьгеля.
5.2.1 Контаминация(заражение)
Соответствующее количество откаждой партии должно быть проверено на контаминацию (заражение).
5.2.2Контрольные микроорганизмы
Набор контрольных организмовдолжен содержать микроорганизмы только со стабильными характеристикамиопределенного вида, которые дают надежные результаты оптимальной эффективностис определенными, приготовленными в лаборатории культуральными средами.Контрольные организмы должны, прежде всего, включать культуры, которые являютсяшироко доступными в коллекциях эталонных культур и являются хорошоохарактеризованными. Хорошо охарактеризованные микроорганизмы, выделенные влаборатории, допускается включать в набор контрольных микроорганизмов. Их культуральныехарактеристики должны быть исследованы и зарегистрированы лабораторией. Вконтрольном наборе должен находиться штамм с атипичными характеристиками.Предпочтительно использовать штаммы, выделенные из пищевых продуктов, хотя невсе коллекции культур предоставляют информацию, касающуюся их происхождения.
Контрольные организмы для каждойсреды могут включать:
- четко положительные штаммы стипичными характеристиками;
- слабо растущие положительныештаммы (то есть более чувствительные по происхождению);
- биохимически не активныештаммы, например демонстрирующие различные реакции ферментации илифлюоресценции;
- полностью ингибированныештаммы.
Примечание - Международныйкомитет по микробиологии и гигиене пищевых продуктов (WPCM) описали утвержденный переченьколлекции штаммов для оценки питательных сред [1].
5.2.3 Готовые к использованиюпитательные среды и реактивы
Изготовители имеющихся в продаже готовых к использованию культуральныхсред особенно те, которые одобрены ИСО 9001 [2] или ИСО9002 [3],имеют программу контроля качества на месте и могут выдавать сертификат качествана культуральные среды, которые они поставляют. При этих условиях пользовательне обязан выполнять обширный объем испытаний приобретенных сред. Необходиматолько гарантия, что поддерживаются необходимые условия хранения.
5.2.4Среды, приготовленные из коммерчески доступных сухих (обезвоженных)ингредиентов
Качественные тесты на каждуюпартию приготовленной среды являются минимальными. Для тех сред, которые несодержат никаких индикаторов или селективных веществ, использование одного положительногоконтрольного штамма в испытании является достаточным. Для тех сред, которыесодержат индикаторы или селективные агенты, должны использоваться штаммы,которые выявляют функцию индикатора или селективности. Для сложных сред, тоесть питательных сред с использованием добавок, каждую партию необходимопроверить со штаммами, характеристики которых приведены в 5.2.2. В случае готовых к использованиюсред, к которым добавляют ингредиенты, приготовленные в лаборатории, используюттот же принцип для проверки.
5.2.5 Среды, приготовленныеиз основных индивидуальных компонентов
Рекомендуется, чтобы вдополнение к качественным тестам, описанным в 5.2.4,выполнялись некоторые количественные исследования при использовании методовтипа модифицированной методики Майлса и Мисра (Miles and Misra) [1]или посева на чашки по спирали, чтобы проследить тенденции качества основныхматериалов, продуктивность питательной среды и последовательность этаповприготовления сред внутри лаборатории.
Примечание - В практикепищевые продукты могут содержать микроорганизмы, подвергнутые стрессу. В связис этим необходимо принимать в расчет способность среды оживления такихнаходящихся под стрессом микроорганизмов. Информацию по методам консервации иподдержанию культуральных сред и коллекций эталонных штаммов см. в приложении В.
Приложение А
(справочное)
А.1 Общие положения
С целью гармонизации описанияразличных ингредиентов в составе культуральных сред в стандартныхмикробиологических методах ИСО/ТС 34/SC 9 «Продовольствие исельскохозяйственные изделия. Микробиология» приняли решение в отношенииобозначений для категории компонентов, представленных в пунктах А.2-А.5.
А.2 Пептоны:
- гидролизат казеинаферментативный2);
- перевар (гидролизат) соиферментативный;
- перевар (гидролизат) тканейживотных ферментативный3);
- перевар (гидролизат) сердцаферментативный;
- перевар (гидролизат) желатинаферментативный;
- перевар (гидролизат) ткани животногои ткани растения ферментативный.
2) Включает пептическийперевар казеина, триптический перевар казеина и триптон.
3)Включает мясной пептон, пептический гидролизат мяса, панкреатический гидролизатмяса.
А.3 Экстракты:
- мясной экстракт;
- сердечно-мозговой экстракт;
- дрожжевой экстракт;
- желчь говяжья длямикробиологии;
- желчные соли;
- желчные соли № 3;
А.4 Агар:
бактериологический агар-агар
А.5 Другие:
- эмульсия яичного желтка;
- сухое обезжиренное(порошковое) молоко;
- кислотный гидролизат казеина.
Приложение В
(справочное)
В.1 Общие положения
Есть несколько доступныхметодов, то есть лиофилизация, хранение на шариках при температуре 70 °С или сиспользованием жидкого азота для успешного сохранения и поддержания всехмикроорганизмов, используемых в ликробиологии пищевых продуктов. При этом несуществует единственного метода сохранения и поддержания контрольных штаммовдля всех штаммов коллекции, использующихся в исследованиях (см. рисунок В.1).
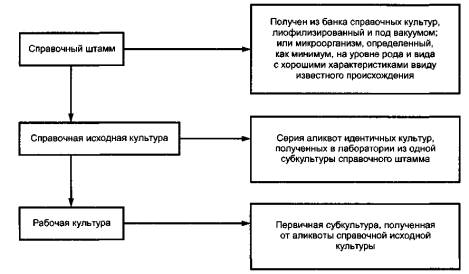
Рисунок В.1
В.2 Контрольные (референс)штаммы из коммерческих источников
Если контрольные (референс)штаммы получены из референс (контрольных) коллекций или поставщиков,сертифицированных ИСО 9001 [2] или ИСО9002 [3],то их использование в отношении культивирования должно осуществляться всоответствии с указаниями производителя или поставщика коллекции.
В.3 Референс (контрольные)наборы, приготовляемые в лаборатории
Наборы культур контрольных(референс) штаммов (см. В.2) для контроля качества и определения эффективностиследует поддерживать и сохранять таким образом, чтобы свести к минимумувозможность заражения, мутации или изменения типичных характеристик.Контрольные наборы следует поддерживать в многочисленных образцах (аликвотах)или свежезамороженными (минус 70 °С) или лиофилизированными. Их ростовыехарактеристики должны быть полностью документированными для каждой среды, на/вкоторой они будут использоваться в качестве контрольных микроорганизмов.
В.4 Рабочие культуры
Рабочие культуры готовят излиофилизированных или свежезамороженных образцов контрольных наборов (см. В.3).Определенные количества должны быть обработаны таким образом, чтобы избежатьвозможной контаминации контрольного набора и ухудшения его ростовых характеристик.Рабочие культуры должны быть приготовлены посредством суспендирования образцаконтрольного набора в неселективную культуральную среду, инкубируя его додостижения роста культуры до стационарной фазы.
Имеющиеся в продаже системыконсервации культур должны иметь инструкцию по поддержанию, сохранению ипринципам работы с рабочими культурами.
Примечание - Из рабочихкультур не должны приготовляться субкультуры. Однако рабочие культурыдопускается использовать неоднократно в течение не более одной недели, если ониобработаны и хранятся таким образом, что исключается возможность перекрестногозаражения или ухудшения их ростовых характеристик.
Таблица С.1
| Неверное отклонение | Возможная причина |
| Агаризованная среда не способна затвердеть | Перегревание среды во время приготовления. Низкое значение рН, вызывающее кислотный гидролиз. Использована неправильная навеска используемого агара. Агар неполностью расплавлен. Плохое перемешивание компонентов среды |
| Неправильное значение рН среды | Перегревание среды во время приготовления. Плохое качество воды. Загрязнение химическими веществами извне. рН измерен при неправильной температуре. рН измерен на неправильно калиброванном рН-метре. Низкое качество сухой (обезвоженной) среды |
| Неправильный цвет | Перегревание среды во время приготовления. Плохое качество воды. Низкое качество сухой (обезвоженной) среды. Неправильное значение рН. Загрязнение среды посторонними ингредиентами |
| Формирование преципитатов | Перегревание среды во время приготовления. Плохое качество воды. Низкое качество сухой (обезвоженной) среды. Плохой контроль рН |
| Ингибирование роста микроорганизмов средой/Низкая продуктивность | Перегревание среды во время приготовления. Низкое качество сухой (обезвоженной) среды. Плохое качество воды. Неправильное использование прописи среды, т.е. ингредиентов, взвешенных неправильно, и добавок, введенных в неправильной концентрации |
| Плохая избирательность (селективность) | Перегревание среды во время приготовления. Низкое качество сухой (обезвоженной) среды. Неправильное использование прописи среды. Добавки внесены неправильно, т.е. среда в чрезмерно высокой или низкой концентрации |
[1]Culture media for Food Microbiology. Progress in Industrial Microbiology,vol.34 (1995)/Eds. Corry J.E.L, Curtis, G.D.W. and Baird, R.M. Elsevier,Amsterdam
[2] ИСО 9001:2000 Системы управления качеством.Требования
[3] ИСО 9002:2000 Системы качества. Модельобеспечения качества при производстве, установке и обслуживании
[4] ЕН 1659:1996 Системы для диагностики in vitro. Культуральные средыдля микробиологических целей. Термины и определения
[5] ЕН 12322:1999 Средства медицинские для диагностики in vitro. Культуральные средыдля микробиологических целей. Критерии эффективности культуральных сред
[6] ИСО 8402:1994 Управление качеством и обеспечение качества. Словарь
Ключевые слова: пищевые продукты, корма, микроорганизмы,культуральные среды, штамм микроорганизмов, жидкие среды, сухие среды, агар,приготовление культуральных сред
Новости
Календарь событий
Библиотека
Soft по ОТ и ПБ
Консультации
Агрегатор
Услуги
Форум
Золотой фонд
ССОТ








