ГОСТ 30347-97
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
МОЛОКО И МОЛОЧНЫЕ ПРОДУКТЫ
МЕТОДЫ ОПРЕДЕЛЕНИЯ
STAPHYLOCOCCUS AUREUS
МЕЖГОСУДАРСТВЕННЫЙ СОВЕТ
ПО СТАНДАРТИЗАЦИИ, МЕТРОЛОГИИ И СЕРТИФИКАЦИИ
Минск
Предисловие
1РАЗРАБОТАН Всероссийским научно-исследовательским институтом мяснойпромышленности (ВНИМИ) и Межгосударственным и техническим комитетом постандартизации МТК 186 «Молоко и молочные продукты»
ВНЕСЕН Госстандартом Российской Федерации
2 ПРИНЯТ Межгосударственным советом по стандартизации,метрологии и сертификации(протокол № 11 от 25 апреля 1997 г.)
За принятие проголосовали:
| Наименование государства | Наименование национального органа по стандартизации |
| Азербайджанская Республика | Аз госстандарт |
| Республика Армения | Армгосстандарт |
| Республика Беларусь | Госстандарт Беларуси |
| Киргизская Республика | Киргизстандарт |
| Республика Молдова | Молдовастандарт |
| Российская Федерация | Госстандарт России |
| Республика Таджикистан | Таджикгосстандарт |
| Туркменистан | Главная государственная инспекция Туркменистана |
| Республика Узбекистан | Узгосстандарт |
| Украина | Госстандарт Украины |
3 Постановлением Государственного комитета Российской Федерациипо стандартизации, метрологии и сертификации от 25 сентября 1997 г. № 341межгосударственный стандарт ГОСТ 30347-97 введен в действие непосредственно вкачестве государственного стандарта Российской Федерации с 1 июля 1998 г. справом досрочного введения
4 ВВЕДЕН ВПЕРВЫЕ
5 ПЕРЕИЗДАНИЕ. Июль 2000 г.
Содержание
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
| МОЛОКО И МОЛОЧНЫЕ ПРОДУКТЫ Методы определения Staphylococcus aureus Milk and milk products. Methods for determination of staphylococcus aureus |
Дата введения 1998-07-01
Настоящий стандартраспространяется на молоко и молочные продукты, закваски, бактериальныеконцентраты и препараты и устанавливает два метода определения Staphylococcus aureus в определенном объеме илинавеске продукта - определение количества с предварительным обогащением;определение количества без предварительного обогащения.
Методопределения Staphylococcus aureus с предварительнымобогащением основан на высеве навески продукта и разведении его в жидкую селективнуюсреду, инкубировании посевов, учете положительных пробирок (колб), пересеве наплотные селективные среды с последующим подтверждением принадлежности выросшихколоний к Staphylococcus aureus.
Методопределения количества Staphylococcus aureus безпредварительного обогащения посевом на агаризованные селективные среды основанна высеве продукта или разведении его на поверхности плотной среды,инкубировании, подсчете типичных колоний Staphylococcus aureus споследующим подтверждением выросших колоний к Staphylococcus aureus поплазмокоагулирующей способности.
В настоящемстандарте использованы ссылки на следующие стандарты:
ГОСТ9225-84 Молоко и молочные продукты. Методы микробиологического анализа
ГОСТ10444.11-89 Продукты пищевые. Методы определения молочнокислыхмикроорганизмов
ГОСТ27583-88 Яйца куриные пищевые. Технические условия
* См. примечание ФГУП «СТАНДАРТИНФОРМ»(с. 8).
3.1 Аппаратура,материалы, реактивы по ГОСТ9225 со следующими дополнениями:
сухая плазмакроличья, цитратная;
контрольныйштамм Staphylococcus aureus;
мембранныефильтры;
калия теллурит[2],раствор с массовой концентрацией 10 г/дм3;
глицин [1],раствор с массовой концентрацией 200 г/дм3;
кристаллическийфиолетовый [6];
натрия пируват[8],раствор с массовой концентрацией 200 г/дм3;
литийхлористый, гексагидрат [4];
триптон;
экстрактдрожжевой [3] или
экстрактдрожжевой, очищенный [7];
экстрактмясной;
фуксин основной[5],спиртовой раствор с массовой концентрацией 50 г/дм3;
яйца куриныепищевые по ГОСТ27583;
витаминныйпрепарат «ЭКД» сухой [11].
3.2 Питательные среды
3.2.1Гидролизованное и стерильное обезжиренное молоко по ГОСТ10444.11 (3.3.1 и 3.3.3).
3.2.2Среды питательные сухие для определения Staphylococcus aureus [9]или питательный агар для культивирования микроорганизмов сухой и питательныйагар сухой II, выпускаемые Дагестанским НПО «Питательные среды» [10].
3.2.3Желточную эмульсию готовят следующим образом.
Свежее куриноеяйцо моют водопроводной водой, затем протирают ваткой, смоченной в спирте, иобсушивают. Отделяют желток и вносят его в 100 см3 стерильногораствора хлористого натрия по ГОСТ9225. Тщательно перемешивают. Приготовленная эмульсия может храниться притемпературе 0-5 °С не более 72 ч.
3.2.4 Солевой бульон*:
Состав: натрийхлористый (NaCl) - 7,5 г;
питательный сухой бульон -1,5 г;
или гидролизованное молоко -100 см3.
Приготовление:в 100 см3 дистиллированной воды вносят 1,5 г сухого питательногобульона, кипятят 1-2 мин, фильтруют через ватный тампон, добавляют 7,5 г NaCl,устанавливают рН (6,9 ± 0,1).
Разливают впробирки или колбы и стерилизуют при температуре (121 ± 1) °С в течение (10 ±1) мин.
Или к 100 см3гидролизованного молока добавляют 7,5 г NaCl, устанавливают рН (6,9 ±0,1), разливают и стерилизуют, как указано выше.
3.2.5Желточно-солевой агар**
Состав: питательный агар***
для культивированиямикроорганизмов (на основе гидролизата кильки) [10]- 35 г
или
питательный агар II***
(на основе гидролизатакормовых дрожжей) [10]- 24 г;
натрий хлористый (NaCl) -75 г;
эмульсия желточная - 50,0 см3;
вода дистиллированная - 1 дм3.
Приготовление:в 1 дм3 дистиллированной воды вносят 36 г питательного агара длякультивирования микроорганизмов или 24 г питательного агара сухого II,добавляют 75 г хлористого натрия (NaCl), кипятят до полногорасплавления агара, фильтруют через ватный тампон, разливают во флаконы иликолбы и стерилизуют при температуре (121 ± 1) °С в течение (20 ± 1) мин. Послестерилизации охлаждают до температуры (45 ± 1) °С и добавляют 50 см3предварительно подготовленной желточной эмульсии. Смесь тщательно перемешиваюти разливают в чашки Петри. Чашки со средой хранят в холодильнике не более 5сут.
3.2.6 Молочно-солевой агар**
Состав: питательный агар*** для культивированиямикроорганизмов (на основе гидролизата кильки) [10]- 35 г
или питательныйагар II*** (на основе гидролизата кормовых дрожжей) [10]- 24,0 г; натрий хлористый (NaCl) - 75,0 г;
молокообезжиренное - 100 см3;
водадистиллированная - 1 дм3.
Приготовление:среду готовят, указано в 3.2.5,но после охлаждения до температуры (45 ± 1) °С добавляют вместо желточнойэмульсии 100 см3 стерильного обезжиренного молока. Смесь тщательноперемешивают и разливают в чашки Петри. Чашки со средой хранят в холодильникене более 5 сут.
3.2.7 Агар Байрд-Паркера *4
Состав.Основа среды:
триптон - 10,0 г;
дрожжевой экстракт [3]- 1,0 г;
* Допускается применениесолевого бульона [9],который готовится согласно указанию на этикетке.
** Допускается использоватьсолевой агар [9],который готовится согласно указанию на этикетке и к которому после стерилизациидобавляется желточная эмульсия или обезжиренное молоко.
*** При изменении заводом-изготовителемколичества вносимой среды на 1 дм дистиллированной воды, количество средывносится согласно указанию на этикетке.
*4Допускается использовать агар Байрд-Паркера [9].Среда готовится согласно указанию на этикетке.
мясной экстракт - 5,0 г;
литий хлористый, гексагидрат[4] -5,0 г;
агар - 12,0-20,0 г;
вода дистиллированная - 1 дм3.
Раствор пирувата натрия:
пируват натрия [8]- 20,0 г;
вода дистиллированная - 100см3.
Раствор глицина:
глицин [1] - 20,0 г;
вода дистиллированная -100,0 см3.
3.2.7.1Приготовление основы среды: в 1 дм3 дистиллированной воды вносят 10г триптона, 5 г мясного экстракта, 1 г дрожжевого экстракта, 5 г хлористоголития, 20 г агара.
При отсутствиитриптона применяют гидролизат казеиновый сухой, а при отсутствии дрожжевогоэкстракта применяют витаминный препарат - «ЭКД» сухой [11].
При отсутствиимясного экстракта, триптона и дрожжевого экстракта вместо дистиллированной водыприменяют 1 дм3 мясопептонного бульона или питательный агар длякультивирования микроорганизмов сухой или питательный агар сухой II [10].
Все компоненты,внесенные в 1 дм3 дистиллированной воды (мясопептонный бульон),нагревают и перемешивают до полного растворения, охлаждают до температуры 50-60°С. Устанавливают рН (7,2 ± 0,1), разливают в колбы или бутылки по 90 см3и стерилизуют при температуре (121 ± 1) °С в течение (20 ± 1) мин.
Прииспользовании сухой среды в 1 дм3 дистиллированной воды вносят 36 гпитательного агара для культивирования микроорганизмов или 24 г питательногоагара сухого II, добавляют 5 г хлористого лития. Нагревают до полногорастворения, охлаждают до температуры 50-60 °С, устанавливают рН (7,2 ± 0,1),разливают и стерилизуют, как указано выше.
Готовую основусреды хранят не более 30 сут при температуре (6 ± 2) °С.
3.2.7.2Перед использованием к 90 см3 расплавленной основы среды добавляютасептически стерилизованные фильтрованием через мембранный фильтр растворы: 6,3см3 раствора глицина, 5 см3 раствора пирувата натрия; 1см3 раствора теллурита калия; 5 см3 желточной эмульсии.
Допускаетсярастворы глицина, пирувата натрия, теллурита калия и желточную эмульсиюготовить в асептических условиях на стерильной дистиллированной воде.
Послетщательного перемешивания приготовленную среду разливают в чашки Петри.
Чашки со средойможно хранить не более 48 ч.
4.1 Приготовление растворов и реактивов
4.1.1 Раствор плазмыкроличьей цитратной готовится согласно инструкции по применению плазмы,прилагаемой к упаковке.
4.1.2Растворы и реактивы для окраски препаратов готовят по ГОСТ9225.
4.1.3Приготовление реактивов для окраски по Грому
4.1.3.1 Приготовление реактива 1
В 100 см3этилового спирта растворяют 0,5 г кристаллического фиолетового [6].
4.1.3.2Приготовление реактива 2
К 96 см3спиртового раствора йодистого калия массовой концентрацией 5 г/дм3добавляют 2 см3 спиртового раствора основного фуксина [5]массовой концентрацией 50 г/дм3 и 2 см3 спиртовогораствора йода массовой концентрацией 50 г/дм3.
Йодистый калийрастворяют в спирте на водяной бане при температуре (45 ± 5) °С при постоянномпомешивании.
4.2Отбор и подготовка проб по ГОСТ9225.
5.1 Метод определения количества Staphylococcus aureus спредварительны м обогащением
5.1.1 Подготовкаи проведение контроля
5.1.1.1 Изнавески продукта готовят ряд десятикратных разведений по ГОСТ9225 так, чтобы можно было определить наличие или отсутствие Staphylococcus aureus в определенной массе(объеме), указанной в нормативном документе на конкретный продукт.
5.1.1.2Навеску продукта или его разведения засевают по 1 см3 в пробирки иликолбочки с солевым бульоном (3.2.4).
Соотношениемежду количеством высеваемого продукта или его эквивалентным разведением ипитательной средой 1 : 10.
Пробирки и колбочкис посевами выдерживают в термостате при температуре (37 ± 1) °С в течение 24 ч.
5.1.1.3Для подтверждения принадлежности микроорганизмов, выросших на солевом бульоне,кStaphylococcus aureus делают пересев петлей избульона для получения изолированных колоний на чашки Петри с подсушеннымисредами типа Байрд-Паркера (3.2.7),желточно-солевой агар или молочно-солевой агар (3.2.5; 3.2.6).
Чашки спосевами выдерживают в термостате при температуре (37 ± 1) °С в течение 24-48ч.
5.1.1.4После термостатирования посевы просматривают и отмечают рост характерныхколоний.
На желточно-солевомагаре колонии Staphylococcus aureus имеют форму плоских дисковдиаметром 2-4 мм белого, желтого, кремового, лимонного, золотистого цвета сровными краями; вокруг колоний образуется радужное кольцо и зона помутнениясреды.
Намолочно-солевом агаре колонии Staphylococcus aureus растутв виде непрозрачных круглых колоний, окрашенных от белого до оранжевого цвета,диаметром 2-4 мм, слегка выпуклых.
На средеБайрд-Паркера колонии Staphylococcus aureus растутв виде черных, блестящих, выпуклых колоний диаметром 1-1,5 мм, окруженных зонойпросветления среды шириной 1-3 мм.
5.1.1.5С каждой чашки Петри отбирают не менее пяти характерных колоний и пересеиваютна поверхность скошенного питательного агара, как указано в 3.2.5, но без добавления хлористогонатрия и желточной эмульсии.
Посевывыдерживают в термостате при температуре (37 ± 1) °С в течение 24 ч. У выросшихколоний определяют отношение к окраске по Граму и коагулированию плазмыкролика.
5.1.1.6Из пяти изолированных, характерных для Staphylococcus aureus колоний,делают препараты, окрашивают по Граму и микроскопируют.
Дляприготовления препарата на чистое и охлажденное после фламбирования предметноестекло наносят петлей каплю дистиллированной воды, в которую вносят петлейнебольшое количество агаровой культуры, не размешивая в воде. Затем вносятпетлей каплю реактива 1, приготовленного по 4.1.3.1. Смесь распределяют научастке примерно 1 см2, просушивают при температуре (20 ± 2) °С ификсируют, медленно пронося предметное стекло над пламенем горелки. На одномстекле можно готовить по шесть - восемь мазков, отделяя их один от другоголиниями, проведенными с лицевой стороны стекла.
Препаратополаскивают водой и тщательно просушивают фильтровальной бумагой.
Послепросушивания на препарат наносят с избытком реактив 2, приготовленный по4.1.3.2 так, чтобы жидкость покрыла всю поверхность стекла. Продолжительностьокрашивания 0,5 -1 мин. После окрашивания препарат быстро ополаскиваютпроточной водой, направляя струю под углом на стекло, помещенное вертикально.Препарат просушивают фильтровальной бумагой и просматривают под микроскопом с иммерсионнойсистемой. Микробы, красящиеся по Граму, будут темно-фиолетового цвета, некрасящиеся по Граму - красного цвета.
Стафилококкиокрашиваются по Граму положительно (темно-фиолетового цвета), имеютшарообразную форму и располагаются скоплениями, чаще всего напоминающимигроздья винограда.
5.1.1.7Постановка реакции плазмокоагуляции
В пробирку с0,5 см3 разведенной кроличьей плазмы вносят петлю суточной агаровойкультуры. Внесенную культуру тщательно размешивают. Одну пробирку с плазмойоставляют незасеянной, а в другую засевают контрольный штамм Staphylococcus aureus (коагулазоположительныйстафилококк). Пробирки помещают в термостат и выдерживают при температуре (37 ±1) °С в течение 3-6 ч. Если через 6 ч коагуляции плазмы не произошло, тооставляют эти пробирки до 24 ч. Если через 24 ч плазма не свернулась, тоиспытуемую культуру стафилококка относят к коагулазоотрицательной.
При определениикоагулазной активности реакцию считают отрицательной в тех случаях, когда вплазме не образуются отдельные нити или сгустки, или в тех случаях, когда вплазме появились отдельные нити (реакцию плазмокоагуляции оценивают на одинплюс).
Реакцию считаютположительной, если:
+ + + + -сгусток плотный;
+ + + -сгусток, имеющий небольшой отсек;
+ +- сгусток в виде взвешенного мешочка.
Все триварианта являются положительным результатом.
При полученииположительной реакции считают, что в посевах обнаружен Staphylococcus aureus.
5.1.2Обработка результатов контроля
Результатыоценивают по каждой пробе отдельно.
5.1.3Оформление результатов контроля
Морфологические,культуральные свойства и положительная реакция плазмокоагуляции свидетельствуюто присутствии коагулазоположительных стафилококков в засеянной массе продукта.
5.2 Метод определения количества Staphylococcus aureus безпредварительного обогащения
5.2.1Проведение контроля
5.2.1.11 см3 жидкого продукта или его разведения (5.1.1) наносят наповерхность питательных сред (3.2.5 или 3.2.6 или 3.2.7) в 3 чашки Петри, тщательнорастирают шпателем по поверхности питательной среды. Посевы инкубируют притемпературе (37 ± 1) °С в течение 24-48 ч. Чашки Петри с посевами инкубируютдном вверх.
5.2.1.2После термостатирования подсчитывают количество характерных колоний на каждойчашке Петри (5.1.4). С каждой чашки Петри отбирают не менее пяти характерныхи/или подозрительных колоний Staphylococcus aureus,а в случае роста менее пяти - все колонии характерные для Staphylococcus aureus и пересевают на поверхностьскошенного питательного агара, разлитого в пробирки, как указано в 3.2.5, но без добавленияхлористого натрия и желточной эмульсии. Пробирки с посевами выдерживают втермостате при температуре (37 ± 1) °С в течение 24 ч.
У выросшихкультур определяют отношение к окраске по Граму и коагулированию плазмы кроликав соответствии с требованиями 5.1.6 и 5.1.7.
5.2.2Обработка результатов контроля
Результатыоценивают по каждой пробе отдельно.
Если приизучении характерных колоний в 80 % случаев, то есть не менее чем в 4 из 5колоний подтвержден рост Staphylococcus aureus,то считают, что все характерные колонии, выросшие на чашках Петри (5.1.7),принадлежат к Staphylococcus aureus. В остальных случаяхколичество Staphylococcus aureus определяют, исходя изпроцентного отношения подтвержденных колоний к общему количеству характерныхколоний, взятых для подтверждения.
5.2.3Оформление результатов контроля
Количествоколоний Staphylococcus aureus в 1 г или 1 см3Хпосле определения его в определенной навеске продукта вычисляют по формуле
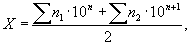 (1)
(1)
где 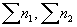 - количество колоний,выросших на всех чашках Петри в пределах одного разведения или засеянногообъема;
- количество колоний,выросших на всех чашках Петри в пределах одного разведения или засеянногообъема;
п - число десятикратныхразведений.
Пример:
Подсчитываемколичество колоний Staphylococcus aureus, выросших на трех засеянныхчашках при посевах продукта или его разведений:
1 гили 1 см3 продукта - 84 96 72
10-1разведение - 9 10 7
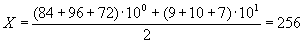 (2)
(2)
10-1разведение - 84 96 72
10-2разведение - 99 10 7
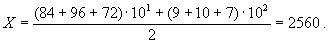 (3)
(3)
[1] ТУ 6-09-09-200-84 Глицин для медицинских целей
[2] ТУ 6-09-2060-77 Калий теллуристокислый водный
[3] ТУ 6-09-3462-73 Экстракт дрожжевой. Технические условия
[4] ТУ 6-09-3751-83 Литий хлорид 1-водный. Технические условия
[5] ТУ 6-09-3804-82 Фуксин основной для микробиологических целей.Технические условия
[6] ТУ 6-09-4119-75 Кристаллический фиолетовый. Технические условия
[7] ТУ 6-09-4510-77 Экстракт дрожжевой очищенный. Технические условия
[8] ТУ 6-09-08-990-75 Натрий пировинограднокислый. Технические условия
[9] ТУ 10-02-02-789-176-94 Среды питательные сухие для определения Staphylococcus aureus. Технические условия
[10]ОКП 93 8511 0197 ФС 42-188 ВС-88 Питательный агар для культивирования микроорганизмовсухой и питательный агар сухой II, выпускаемые ДагестанскимНПО «Питательные среды»
[11]ОКП 93 85630197 ФС 42386 ВС-91 Витаминный препарат «ЭКД» сухой
Ключевыеслова:питательные среды, коагулазоположительные стафилококки, характерные колонии,окраска по Граму, коагулирование плазмы
ПРИМЕЧАНИЕФГУП «СТАНДАРТИНФОРМ»
Указанный вразделе 2 «Нормативные ссылки» к ГОСТ 30347-97:
ГОСТ27583-88. На территории Российской Федерации действует ГОСТ Р 52121-2003. Яйцакуриные пищевые. Технические условия
Новости
Календарь событий
Библиотека
Soft по ОТ и ПБ
Консультации
Агрегатор
Услуги
Форум
Золотой фонд
ССОТ





.webp)




