Государственное
санитарно-эпидемиологическое нормирование
Российской Федерации
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Измерение концентраций гербицидов
различных классов при совместном
присутствии в воздушной среде
и воде водоемов
хроматографическими методами
Методические указания
МУК 4.1.3085-13
Москва
2013
Федеральная служба по надзору в сфере
защиты
прав потребителей и благополучия человека
1. Разработаны
ФБУН «Федеральный научный центр гигиены им. Ф.Ф. Эрисмана» Роспотребнадзора
(В.Н. Ракитский, Т.В. Юдина, Н.Е. Федорова, В.Н. Волкова, М.В. Ларькина, М.В. Егорова. Л.В.
Горячева, О.Е. Егорченкова, С.К. Рогачева, Л.П. Мухина, В.М. Волков).
2. Рекомендованы к
утверждению Комиссией по государственному санитарно-эпидемиологическому
нормированию при Федеральной службе по надзору в сфере защиты прав потребителей
и благополучия человека (протокол от 30 мая 2013 г. № 1).
3. Утверждены
Руководителем Федеральной службы по надзору в
сфере защиты прав потребителей и благополучия человека, Главным государственным
санитарным врачом Российской Федерации Г.Г. Онищенко 29 июля 2013 г.
4. Введены
впервые.
СОДЕРЖАНИЕ
|
УТВЕРЖДАЮ
Руководитель Федеральной
службы
по надзору в сфере защиты прав
потребителей и благополучия
человека,
Главный государственный
санитарный
врач Российской Федерации
Г.Г. Онищенко
29 июля 2013 г.
Дата
введения: с момента утверждения
|
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Измерение концентраций гербицидов
различных классов при совместном присутствии
в воздушной среде и воде водоемов
хроматографическими методами
Методические
указания
МУК 4.1.3085-13
Свидетельство о метрологической аттестации
от 14.08.2012 № 0123.24.08.12
Настоящие методические
указания устанавливают порядок применения методов высокоэффективной жидкостной
хроматографии для измерения концентраций биспирибака кислоты, имазапира, имазетапира,
метсульфурон-метила, никосульфурона, пеноксулама,
сульфометурон-метила, тифенсульфурон-метила,
топрамезона и трифлуфульфурон-метила в воде в
диапазоне 0,0005 - 0,005 мг/дм3, атмосферном воздухе - 0,0016
- 0,016 мг/м3;
воздухе рабочей зоны - 0,25 - 2,5 мг/м3 и газожидкостной
хроматографии для измерения концентраций 2,4-Д, МСРА (МЦПА), аминопиралида,
ацетохлора, ацифлуорфена, бентазона, дикамбы, клопиралида и пиклорама в воде в диапазоне 0,0001 - 0,001 мг/дм3,
атмосферном воздухе - 0,00008 - 0,0008 мг/м3, воздухе рабочей зоны -
0,1 - 1,0 мг/м3.
Методические указания носят
рекомендательный характер.
Характеристика веществ,
основные физико-химические свойства представлены в табл. 1.
При соблюдении всех
регламентированных условий проведения анализа в точном соответствии с данной
методикой погрешность (и её составляющие) результатов измерений при
доверительной вероятности Р = 0,95 не превышает значений, приведенных в табл. 2 (вода), 3 (атмосферный воздух), 4 (воздух рабочей зоны) для
соответствующих диапазонов концентраций.
Таблица 1
Характеристика веществ, основные
физико-химические свойства
|
Вещество, химическое наименование
|
Брутто-формула, молекул. масса
|
Температура плавления, °С
|
Давление паров, мПа (при t, °С)
|
Растворимость в воде, г/дм3 (20 - 25 °С)
|
|
1
|
2
|
3
|
4
|
5
|
|
2,4-Д
(2,4-дихлорфенокси)уксусная
кислота
|
С8Н6С12O3
221,0
|
140
|
1,86×10-2(25)
|
0,311 (рН
1);
20,031 (рН
5);
23,180 (рН
7);
34,196 (рН
9)
|
|
МСРА
(4-хлор-2-метокси-фенокси)уксусная кислота
|
С9Н9ClO3
200,6
|
119 - 120
|
2,3×10-2 (20)
0,4(32)
|
0,395 (рН 1);
0,0262 (рН 5);
0,2739 (рН
7);
0,3201 (рН
9)
|
|
Аминопиралид
4-амино-3,6-дихлорпиридин-2-карбо-новая кислота
|
C6H4C12N2O2
207,0
|
163,5 - 165,5
|
9,52×10-6
(20)
|
2,48 (рН 2,35);
203 - 205 (рН 7 - 9)
|
|
Ацифлуорфен
5-(2-хлор-а,а,а-трифтор-ляря-толи-локси)-2-нитробензойная кислота
|
C14H7ClF3NO5
361,7
|
142 - 160
|
< 0,01 (20)
|
6,081 (рН 7);
6,071 (рН 9)
|
|
Ацетохлор
2-хлор-N-этоксиметил-6'-этилацето-орто-толуидид
|
c15h19n3O4
269,8
|
10,6
|
2,2×10-2 (20)
|
0,223
|
|
Бентазон
3-изопропил-1H-бензотиадиазин--4(3H)-он,2,2-диоксид
|
C10H12N2O3S
240,3
|
139,4 - 141
|
0,17 (20)
|
0,570 (рН 7)
|
|
Биспирибака кислота
2,6-бис[(4,6-диметоксипиримидин-2--ил)окси] бензойная кислота
|
c19h18n4O8
240,3
|
148 - 150
|
6,47×10-6
(20)
|
0,4
|
|
Дикамба
3,6-дихлор-2-метоксибензойная кислота
|
С8Н6С12O3
221,0
|
114 - 116
|
6,47×10-6
(25)
|
6,1
|
|
Имазапир
2-(4-изопропил-4-метил-5-оксо-2-имидазолин-2-ил)никотиновая кислота
|
C13H15N3O3
261,3
|
169 - 173
|
< 0,013 (60)
|
11,3
|
|
Имазетапир
(RS)-5-этил-2-(4-изопропил-4-метил-5-оксо-2-имидазолин-2-ил)никотиновая
кислота
|
c13h19n3O3
289,3
|
169 - 173
|
< 0,013 (60)
|
1,4
|
|
Клопиралид
3,6-дихлорпиридин-2-карбоновая
кислота
|
C6H3Cl2NO2
190,0
|
151 - 152
|
1,33 (24)
|
118 (pH 5);
143 (pH 7);
157 (pH 9)
|
|
Метсульфурон-метил
2-(4-метокси-6-метил-1,3,5-триазин-2-ил-карбамоилсульфамоил)бензойная
кислота
|
C14H15N5O6S
381,4
|
158
|
1,1×10-7 (25)
|
0,55 (pH
5);
2,79 (pH
7);
213 (pH 9)
|
|
Никосульфурон
1-(4,6-диметоксипиримидин-2-ил)-3-(3-диметил-карбамоил-2-пиридин-сульфонил)мочевина
|
C15H18N6О6S
410,4
|
169 - 172
|
< 8×10-7 (25)
|
0,07
|
|
Пеноксулам
2-(2,2-дифторэтокси)-N-(5,8-диметокси[1,2,4]триазоло[1,5-с]пиримидин-2-ил)-6-(трифторметил)бензолсульфамид
|
C16HI4FN5O5S
483,37
|
212
|
2,5×10-11
(25)
|
0,408
|
|
Пиклорам
4-амино-3,5,6-трихлорпиридин-2-карбоновая кислота
|
C6H4Cl3N2O2
241,5
|
разлагается при 215 (без плавления)
|
8×10-11
(25)
|
0,56
|
|
Сульфометурон-метил
2-(4,6-диметилпиримидин-2-илкарбамоилсульфа-моил)бензойная
кислота, метиловый эфир
|
C15H16N4O5S3
64,4
|
203 - 205
|
7,3×10-11
(25)
|
0,244 (рН 7)
|
|
Тифенсульфурон-метил
3-[(4-метокси-6-метил-1,3,5-тиразин-2-ил)карбамоилсуль-фамоил]тиофен-2-карбоновая
кислота, метиловый эфир
|
Cl2H13N5O6S2
387,4
|
176
|
7,5×10-6
(25)
|
0,23 (рН 5);
6,27 (рН 7)
|
|
Трифлусульфурон-метил
2-[4-диметиламино-6-(2,2,2-трифтор-этокси)-1,3,5-триазин-2-илкарбамоил-сульфамоил]-мета-толуиловая кислота, метиловый
эфир
|
C17H19F3N6O6S
492,4
|
160 - 163
|
6×10-7 (25)
|
0,001 (рН 3);
0,003 (рН 5);
0,110 (рН 7);
11,0 (рН 9)
|
|
Топрамезон
(5-гидрокси-1-метил-1H-пиразол-4-ил)[3-(4,5-дигидроизоксазол-3-ил)-2-метил-4-метилсульфонилфенил]метанон
|
C16H17N3O5S
363,39
|
221,6
|
1,0×10-7
(25)
|
100
|
Таблица 2
Метрологические параметры измерения
концентраций веществ в воде
|
Вещество
|
Диапазон определяемых концентраций, мг/дм3
|
Показатель точности (граница относительной погрешности),
δ, %,
Р = 0,95
|
Показатель повторяемости (среднеквадратичное отклонение
повторяемости), σr, %
|
Предел повторяемости (значение допустимого расхождения
между двумя результатами параллельных определений), r, %
|
Предел воспроизводимости (значение допустимого расхождения
между двумя результатами измерений, полученных в разных лабораториях), R (Р
= 0,95),%
|
|
1
|
2
|
3
|
4
|
5
|
6
|
|
2,4-Д
|
от 0,0001 до 0,001 вкл.
|
50
|
2,5
|
7
|
10
|
|
МСРА
|
от 0,0001 до 0,001 вкл.
|
50
|
1,8
|
5
|
7
|
|
Аминопиралид
|
от 0,0001 до 0,001 вкл.
|
50
|
1,8
|
5
|
7
|
|
Ацифлуорфен
|
от 0,0001 до 0,001 вкл.
|
50
|
2,3
|
6
|
8
|
|
Ацетохлор
|
от 0,0001 до 0,001 вкл.
|
50
|
2,0
|
6
|
8
|
|
Бентазон
|
от 0.0001 до 0,001 вкл.
|
50
|
3,3
|
9
|
13
|
|
Биспирибака кислота
|
от 0,0005 до 0,005 вкл.
|
50
|
2,2
|
6
|
8
|
|
Дикамба
|
от 0,0001 до 0,001 вкл.
|
50
|
2,0
|
6
|
8
|
|
Имазапир
|
от 0,0005 до 0,005 вкл.
|
50
|
2,0
|
6
|
8
|
|
Имазетапир
|
от 0,0005 до 0,005 вкл.
|
50
|
2,5
|
7
|
10
|
|
Клопиралид
|
от 0,0001 до 0,001 вкл.
|
50
|
3,0
|
6
|
8
|
|
Метсульфурон-метил
|
от 0,0005 до 0,005 вкл.
|
50
|
1,8
|
5
|
7
|
|
Нико-сульфурон
|
от 0,0005 до 0,005 вкл.
|
50
|
1,9
|
5
|
7
|
|
Пеноксулам
|
от 0,0005 до 0,005 вкл.
|
50
|
2,1
|
6
|
8
|
|
Пиклорам
|
от 0,0001 до 0,001 вкл.
|
50
|
2,6
|
7
|
10
|
|
Сульфометурон-метил
|
от 0,0005 до 0,005 вкл.
|
50
|
1,9
|
5
|
7
|
|
Тифен-сульфурон-метил
|
от 0,0005 до 0,005 вкл.
|
50
|
1,7
|
5
|
7
|
|
Трифлусульфурон-метил
|
от 0,0005 до 0,005 вкл.
|
50
|
2,9
|
8
|
11
|
|
Топрамезон
|
от 0,0005 до 0,005 вкл.
|
50
|
2,4
|
7
|
10
|
Таблица 3
Метрологические параметры измерения
концентраций веществ в атмосферном воздухе
|
Вещество
|
Диапазон определяемых концентраций, мг/м3
|
Показатель точности (граница относительной погрешности), δ,%, Р =
0,95
|
Показатель повторяемости (среднеквадратичное отклонение
повторяемости), σr, %
|
Предел повторяемости (значение допустимого расхождения
между двумя результатами параллельных определений), r, %
|
Предел воспроизводимости (значение допустимого
расхождения между двумя результатами измерений, полученных в разных
лабораториях), R (Р = 0,95),%
|
|
1
|
2
|
3
|
4
|
5
|
6
|
|
2,4-Д
|
от 0,00008 до 0,0008 вкл.
|
19,4
|
2,5
|
7
|
10
|
|
МСРА
|
от 0,00008 до 0,0008 вкл.
|
18,8
|
1,8
|
5
|
7
|
|
Аминопиралид
|
от 0,00008 до 0,0008 вкл.
|
18,3
|
1,8
|
5
|
7
|
|
Ацифлуорфен
|
от 0,00008 до 0,0008 вкл.
|
21,0
|
2,3
|
6
|
8
|
|
Ацетохлор
|
от 0,00008 до 0,0008 вкл.
|
17,6
|
2,0
|
6
|
8
|
|
Бентазон
|
от 0,00008 до 0,0008 вкл.
|
16,1
|
3,3
|
9
|
13
|
|
Биспирибака кислота
|
от 0,0016 до 0,016 вкл.
|
20,1
|
1,7
|
5
|
7
|
|
Дикамба
|
от 0,00008 до 0,0008 вкл.
|
18,3
|
2,0
|
6
|
8
|
|
Имазапир
|
от 0,0016 до 0,016 вкл.
|
18,8
|
1,8
|
5
|
7
|
|
Имазетапир
|
от 0,0016 до 0,016 вкл.
|
20,1
|
1,6
|
5
|
7
|
|
Клопиралид
|
от 0,00008 до 0,0008 вкл.
|
18,5
|
3,0
|
8
|
11
|
|
Метсульфурон-метил
|
от 0,0016 до 0,016 вкл.
|
20,6
|
1,8
|
5
|
7
|
|
Никосульфурон
|
от 0,0016 до 0,016 вкл.
|
20,4
|
1,7
|
5
|
7
|
|
Пеноксулам
|
от 0,0016 до 0,016 вкл.
|
20,1
|
2,0
|
6
|
8
|
|
Пиклорам
|
от 0,00008 до 0,0008 вкл.
|
17,7
|
2,6
|
7
|
10
|
|
Сулъфометурон-метил
|
от 0,0016 до 0,016 вкл.
|
17,8
|
1,2
|
4
|
6
|
|
Тифенсульфурон-метил
|
от 0,0016 до 0,016 вкл.
|
19,48
|
1,7
|
5
|
7
|
|
Трифлусульфурон-метил
|
от 0,0016 до 0,016 вкл.
|
15,0
|
2,0
|
6
|
8
|
|
Топрамезон
|
от 0,0016 до 0,016 вкл.
|
16,2
|
1,5
|
4
|
6
|
Таблица 4
Метрологические параметры
измерения концентраций веществ в воздухе рабочей зоны
|
Вещество
|
Диапазон определяемых концентраций, мг/м3
|
Показатель точности (граница относительной погрешности), δ, %, Р
= 0,95
|
Показатель повторяемости (среднеквадратичное отклонение
повторяемости), σr, %
|
Предел повторяемости (значение допустимого расхождения
между двумя результатами параллельных определений), r, %
|
Предел воспроизводимости (значение допустимого
расхождения между двумя результатами измерений, полученных в разных
лабораториях), R (Р = 0,95),%
|
|
1
|
2
|
3
|
4
|
5
|
6
|
|
2,4-Д
|
0,1 - 1,0
|
19,4
|
2,5
|
7
|
10
|
|
МСРА
|
0,1 - 1,0
|
18,8
|
1,8
|
5
|
7
|
|
Аминопиралид
|
0,1 - 1,0
|
18,3
|
1,8
|
5
|
7
|
|
Ацифлуорфен
|
0,1 - 1,0
|
21,0
|
2,3
|
6
|
8
|
|
Ацетохлор
|
0,1 - 1,0
|
17,6
|
2,0
|
6
|
8
|
|
Бентазон
|
0,1 - 1,0
|
16,1
|
3,3
|
9
|
13
|
|
Биспирибака кислота
|
0,25 - 2,5
|
20,1
|
1,7
|
5
|
7
|
|
Дикамба
|
0,1 - 1,0
|
18,3
|
2,0
|
6
|
8
|
|
Имазапир
|
0,25 - 2,5
|
15,8
|
1,8
|
5
|
7
|
|
Имазетапир
|
0,25 - 2,5
|
17,3
|
1,6
|
5
|
7
|
|
Клопиралид
|
0,1 - 1,0
|
18,5
|
3,0
|
8
|
И
|
|
Метсульфурон-метил
|
0,25 - 2,5
|
20,6
|
1,8
|
5
|
7
|
|
Никосульфурон
|
0,25 - 2,5
|
20,4
|
1,1
|
5
|
7
|
|
Пеноксулам
|
0,25 - 2,5
|
20,1
|
2,0
|
6
|
8
|
|
Пиклорам
|
0,1 - 1,0
|
17,7
|
2,6
|
7
|
10
|
|
Сульфометурон-метил
|
0,25 - 2,5
|
17,8
|
1,2
|
4
|
6
|
|
Тифенсульфурон-метил
|
0,25 - 2,5
|
19,48
|
1,7
|
5
|
7
|
|
Трифлусульфурон-метил
|
0,25 - 2,5
|
15,0
|
2,0
|
6
|
8
|
|
Топрамезон
|
0,25 - 2,5
|
16,2
|
1,5
|
4
|
6
|
Метод основан на определении
биспирибака кислоты, имазапира, имазетапира, метсульфурон-метила, никосульфурона, пеноксулама, сульфометурон-метила,
тифенсульфурон-метила, топрамезона и
трифлуфульфурон-метила при совместном присутствии в водной и воздушной средах с
использованием обращенно-фазовой высокоэффективной жидкостной хроматографии
(ВЭЖХ) с ультрафиолетовым детектором. Для концентрирования и очистки пробы воды
использованы патроны для твердофазной экстракции. Концентрирование аэрозолей
веществ из воздуха осуществляют на плотный бумажный фильтр, экстракцию с
фильтров выполняют этиловым спиртом. Нижний предел измерения в анализируемом
объеме пробы - 1 нг.
Определение 2,4-Д, МСРА,
аминопиралида, ацетохлора, ацифлуорфена, бентазона, дикамбы, клопиралида и
пиклорама при совместном присутствии в водной и воздушной средах основано на
использовании капиллярной газожидкостной хроматографии (ГЖХ) с детектором электронного
захвата ионов или масс-селективным детектором после экстракции веществ из анализируемых
образцов воды (после подкисления до рН 1) трет-бутил-метиловым эфиром, очистки
экстрактов на концентрирующем патроне на основе силикагеля.
Предварительная обработка
водного образца раствором гидроксида натрия (рН 12, гидролиз эфиров) позволяет
определять вещества, присутствующие в воде в виде их эфиров, солей и кислот.
Газохроматографическому
измерению предшествует стадия дериватизации веществ кислотного типа в метиловый эфир (за
исключением ацетохлора).
Концентрирование веществ из
воздуха осуществляют на пробоотборные трубки, заполненные пористым полимерным
сорбентом, экстракцию с сорбента выполняют ацетоном. Нижний предел измерения в
анализируемом объеме пробы - 0,01 нг.
Количественное определение
проводится методом абсолютной калибровки.
3.1. Средства
измерений
|
Жидкостный хроматограф с быстросканирующим
ультрафиолетовым детектором, снабженный дегазатором, автоматическим
пробоотборником и термостатом колонки
|
|
Газовый хроматограф, снабженный
электронозахватным детектором с пределом детектирования по линдану
3,4×10-14 г/с и масс-селективным автоматическим пробоотборником, предназначенный
для работы с капиллярной колонкой
|
|
Барометр-анероид с
диапазоном измерения атмосферного давления 5 - 790 мм рт.ст.
|
ТУ 2504-1797-75
|
|
Весы лабораторные
аналитические, наибольший предел взвешивания 110 г, предел допустимой погрешности ±0,2 мг
|
ГОСТ
Р 53228-08
|
|
Весы лабораторные общего назначения
с наибольшим пределом взвешивания до 500 г и пределом допустимой погрешности
±0,038 г
|
ГОСТ
Р 53228-08
|
|
Микрошприц вместимостью 10
мм3
|
|
|
рН-метр
|
|
|
Колбы мерные вместимостью
2-50-2,
2-100-2, 2-250-2, 2-1000-2
|
ГОСТ
1770-74
|
|
Меры массы
|
ГОСТ OIML R 111-1-09
|
|
Пипетки градуированные 2-го
класса точности вместимостью 1,0; 2,0; 5,0; 10 см3
|
ГОСТ
29227-91
|
|
Пробоотборное устройство
2-канальное с диапазоном расхода 0,2 - 1,0 и 1,0 - 5,0 дм3/мин
|
|
|
Термометр лабораторный
шкальный, цена деления 1 °С, пределы измерения 0 - 55 °С
|
ТУ 25-2021.003-88
|
|
Цилиндры мерные 2-го класса
точности вместимостью 25, 50, 100, 250, 500 и 1000 см3
|
ГОСТ
1770-74
|
Примечание. Допускается использование средств измерения с аналогичными или лучшими
характеристиками.
3.2. Реактивы
|
2,4-Д, аналитический
стандарт с содержанием основного компонента 99,6%
|
|
|
МСРА (МЦПА), аналитический
стандарт с содержанием основного компонента 99,2 %
|
|
|
Аминопиралид, аналитический
стандарт с содержанием основного компонента 99,9 %
|
|
|
Ацифлуорфен, аналитический
стандарт с содержанием основного компонента 99,9 %
|
|
|
Ацетохлор, аналитический стандарт с
содержанием основного компонента 98,8%
|
|
|
Бентазон, аналитический
стандарт с содержанием основного компонента 99,0%
|
|
|
Биспирибака кислота,
аналитический стандарт с содержанием основного компонента 98,2 %
|
|
|
Дикамба, аналитический
стандарт с содержанием основного компонента 99,8%
|
|
|
Имазапир, аналитический
стандарт с содержанием основного компонента 99,6%
|
|
|
Имазетапир, аналитический
стандарт с содержанием основного компонента 99,3 %
|
|
|
Клопиралид, аналитический
стандарт с содержанием
основного компонента 98,6 %
|
|
|
Метсульфурон-метил,
аналитический стандарт с содержанием основного компонента 98,1 %
|
|
|
Никосульфурон,
аналитический стандарт с содержанием основного компонента 97,3 %
|
|
|
Пеноксулам, аналитический стандарт с
содержанием основного компонента 99,0 %
|
|
|
Пиклорам,
аналитический стандарт с содержанием основного компонента 99,4%
|
|
|
Сульфометурон-метил,
аналитический стандарт с содержанием основного компонента 98,3 %
|
|
|
Тифенсульфурон-метил, аналитический
стандарт с содержанием основного компонента 97,4 %
|
СОП 82-07
|
|
Трифлусульфурон-метил, аналитический
стандарт с содержанием основного компонента 98,1 %
|
СОП
97-08
|
|
Топрамезон, аналитический
стандарт с содержанием основного компонента 99,8 %
|
|
|
Азот газообразный (чистота
99,999%), в баллонах
|
ТУ 6-21-39-96
|
|
Гелий газообразный в.ч., в
баллонах
|
ТУ 0271-001-45905715-02
|
|
Ацетон, ос.ч.
|
ГОСТ 2603-79
|
|
Ацетонитрил для хроматографии,
х.ч.
|
ТУ 6-09-14-2167-84
|
|
Вода дистиллированная
|
ГОСТ 6709-72
|
|
Вода для лабораторного
анализа (деионизованная, бидистиллированная)
|
ГОСТ Р 52501-05
|
|
н-Гексан (гексан), для хроматографии
|
ТУ 6-09-06-657-84
|
|
Калия гидроксид (гидроокись
калия), гранулированный, х.ч.
|
ГОСТ 24363-80
|
|
Калий углекислый (карбонат
калия, поташ), х.ч., прокаленный
|
ГОСТ 4221-76
|
|
Кислота серная
(концентрированная), х.ч.
|
ГОСТ 4204-77
|
|
Кислота ортофосфорная,
х.ч., 85 %
|
ГОСТ 6552-80
|
|
Кислота уксусная, ледяная,
х.ч.
|
ГОСТ 61-75
|
|
Медь серно-кислая
(сульфат), 5-водная
|
ГОСТ 4165-76
|
|
Метиламин гидрохлорид, ч.
|
ТУ 6-09-3755-74
|
|
Мочевина, ч.д.а.
|
ГОСТ 6691-77
|
|
трет-Бутилметиловый эфир, х.ч.
|
ТУ 6-09-3531-84
|
|
Натрий азотисто-кислый
(нитрит натрия), х.ч.
|
ГОСТ 4197-74
|
|
Натрия гидроокись
(гидроксид натрия), х.ч.
|
ГОСТ 4328-77
|
|
Натрий серно-кислый
(сульфат натрия) безводный, х.ч.
|
ГОСТ 4166-76
|
|
Натрий серноватисто-кислый
(тиосульфат), ч.д.а.
|
СТ СЭВ 223-75
|
|
Натрий хлористый, х.ч.
|
ГОСТ 4233-77
|
|
Пропанол-1 (н-пропанол), х.ч.
|
ТУ6-09-4344-77
|
|
Фосфор (V) оксид (фосфорный ангидрид, пентоксид
фосфора)
|
ТУ 6-09-4173-85
|
|
Силикагель для колоночной хроматографии
(размер частиц 0,200 - 0,500 мм)
|
|
|
Спирт этиловый (этанол)
ректификованный
|
ГОСТ
Р 51652-2000
или ГОСТ
18300-87
|
|
Эфир диэтиловый (этиловый
эфир), ч.д.а.
|
ТУ 2600-001-43852015-02
|
Примечание. Допускается
использование реактивов с более высокой квалификацией, не требующих
дополнительной очистки растворителей.
3.3. Вспомогательные средства
измерений, устройства, материалы
|
Аллонж прямой с отводом для
вакуума (для работы с концентрирующими патронами)
|
|
|
Аппарат для встряхивания
проб
|
ТУ
64-1-2851-78
|
|
Баня водяная
|
ТУ 46-22-603-75
|
|
Баня ультразвуковая с
рабочей частотой 35 кГц
|
|
|
Бумага индикаторная
универсальная рН 1-14
|
ТУ 6-09-1181-89
|
|
Бумажные фильтры средней и
высокой плотности
|
ТУ 2642-001-05015242-07
|
|
Воронка Бюхнера
|
ГОСТ
9147-80
|
|
Воронка делительная
вместимостью 500 см3
|
ГОСТ
9737-93
|
|
Воронки химические
стеклянные конусные
|
ГОСТ
25336-82
|
|
Гигрометр с диапазоном
измерений относительной влажности от 30 до 90 %
|
ТУ
25-11-1645-84
|
|
Груша резиновая
|
ТУ 9398-05-0576-9082-03
|
|
Колба Бунзена
|
ГОСТ
25336-82
|
|
Колбы конические (плоскодонные)
с пришлифованной пробкой вместимостью 100, 250 - 300 и 400 - 500 см3
|
ГОСТ
23932-90
|
|
Колбы круглодонные на шлифе (для упаривания)
вместимостью 50, 100, 150 и 1000 см3
|
ГОСТ
9737-93
|
|
Лед
|
|
|
Мешалка магнитная
|
|
|
Набор для фильтрации
растворителей через мембрану
|
|
|
Насос водоструйный
вакуумный
|
|
|
Патроны концентрирующие для твердофазной
экстракции, 60 мг гидрофильно-липофильно
сбалансированного обращенно-фазного сорбента на основе сополимера N- винилпирролидона и дивинилбензола (патрон № 1)
|
|
Патроны концентрирующие для
твердофазной экстракции, 360 мг сорбента на основе силикагеля (патрон № 2)
|
|
|
Пробирки со шлифом
вместимостью 5 и 10 см3
|
ГОСТ
25336-82
|
|
Стаканы химические
вместимостью 100, 150 и 2000 см3
|
ГОСТ
25336-82
|
|
Стекловата
|
|
|
Склянка из темного стекла
|
|
|
Стеклянные палочки
|
|
|
Трубки для отбора проб воздуха,
стеклянные 2-секционные (длиной 100 мм, внутренним диаметром 8 мм),
заполненные пористым полимерным сорбентом на основе 2,6-дифенил-п-фениленоксида (100 мг сорбента во
фронтальной секции, 50 мг - в задней) - пробоотборные трубки
|
|
Ректификационная колонна с
числом теоретических тарелок не менее 30
|
|
|
Ротационный вакуумный
испаритель с мембранным насосом, обеспечивающим вакуум до 10 мбар
|
|
|
Установка для перегонки
растворителей
|
|
|
Холодильник водяной
обратный
|
|
|
Хроматографическая капиллярная кварцевая
колонка длиной 30 м, внутренним диаметром 0,25 мм, содержащая сорбент: 14 %
цианпропилфенил-полисилоксана и 86 % диметилполисилоксана, толщина пленки
сорбента 0,25 мкм
|
|
Хроматографическая капиллярная кварцевая
колонка, длиной 30 м, внутренним диаметром 0,25 мм, содержащая сорбент: 5 %
фенилполисилоксана и 95 % диметилполисилоксана, толщина пленки сорбента 0,25
мкм
|
|
Хроматографическая колонка стальная
длиной 150 мм, внутренним диаметром 4,6 мм, заполненная обращенно-фазным сорбентом с привитыми
монофункциональными полярными группами С18, зернением 5 мкм
|
|
Шприц для ввода образцов
для жидкостного хроматографа вместимостью 50 - 100 мм3
|
|
Примечание. Допускается использование вспомогательных средств
измерений, устройств и материалов с аналогичными или лучшими техническими
характеристиками.
4.1. При выполнении измерений необходимо
соблюдать требования техники безопасности при работе с химическими реактивами
по ГОСТ
12.1.007-76, требования по электробезопасности при работе с
электроустановками по ГОСТ
Р 12.1.019-09, а также требования, изложенные в технической документации на
жидкостный и газовый хроматографы.
4.2. Помещение должно
соответствовать требованиям пожаробезопасности по ГОСТ
12.1.004-91 и иметь средства пожаротушения по ГОСТ
12.4.009-83. Содержание вредных веществ в воздухе на должно превышать ПДК (ОБУВ), установленных ГН
2.2.5.1313-03 и 2.2.5.2308-07.
Организация обучения работников безопасности труда - по ГОСТ
12.0.004-90.
4.3. При работе с газами,
находящимися в баллонах под давлением до 15 МПа (150 кгс/см2),
необходимо соблюдать «Правила устройства и безопасной эксплуатации стационарных
компрессорных установок, воздухопроводов и газопроводов под давлением», ПБ-03-576-03.
Запрещается открывать вентиль баллона, не установив на нем понижающий редуктор.
К выполнению измерений
допускают специалиста, прошедшего обучение, освоившего методику, владеющего
техникой, имеющего опыт работы на жидкостном хроматографе и подтвердившего
соответствие получаемых результатов нормативам контроля погрешности измерений
по п. 12.
При выполнении измерений
соблюдают следующие условия:
· процессы приготовления растворов и
подготовки проб к анализу проводят при температуре воздуха (20 ± 5) °С и
относительной влажности не более 80 %;
· выполнение измерений на жидкостном и
газовом хроматографах проводят в условиях, рекомендованных технической
документацией к прибору.
Измерениям предшествуют
следующие операции: очистка органических растворителей (при необходимости), приготовление
растворов, градуировочных растворов, растворов внесения, смеси растворителей
для растворения проб (метод ВЭЖХ), получение N-нитрозо-N-метилмочевины (при необходимости) и раствора диазометана
(метод ГЖХ), установление градуировочных характеристик, подготовка
концентрирующих патронов, фильтры средней и высокой плотности, отбор проб.
7.1. Очистка органических
растворителей
7.1.1. Ацетон
Ацетон
перегоняют над небольшим количеством перманганата калия и прокаленным карбонатом
калия или подвергают ректификационной перегонке на колонне с числом
теоретических тарелок не менее 30.
7.1.2. Ацетонитрил
Ацетонитрил кипятят с
обратным холодильником над пентоксидом фосфора (на 1 дм3
ацетонитрила 20 г пентоксида фосфора) не менее 1 ч, после чего перегоняют,
непосредственно перед употреблением ацетонитрил повторно перегоняют над
прокаленным карбонатом калия (на 1 дм3 ацетонитрила 10 г карбоната
калия).
7.1.3. н-Гексан
Растворитель последовательно
промывают порциями концентрированной серной кислоты, до тех пор пока она не
перестанет окрашиваться в желтый цвет, затем водой до нейтральной реакции
промывных вод, перегоняют над прокаленным карбонатом калия.
7.2. Приготовление раствора гидроксида
калия с массовой долей 40 % (40 %-й раствор)
В мерную колбу вместимостью
50 см3 помещают (20 ± 0,1) г гидроксида калия, растворяют в 25 - 30
см3 дистиллированной воды, доводят водой до метки.
7.3. Получение N-нитрозо-N-метилмочевины
В отсутствии коммерческого
препарата нитрозометилмочевины осуществляют его синтез.
Все работы необходимо
проводить в вытяжном шкафу!
В круглодонную колбу на шлифе вместимостью 1 дм3,
снабженную обратным холодильником, помещают 80 г метиламина гидрохлорида и 300
г мочевины, растворяют содержимое в 400 см3 воды и кипятят 3 ч с
обратным холодильником на водяной бане. Раствор в колбе охлаждают до комнатной температуры и добавляют в него 110 г нитрита натрия, охлаждают в бане со льдом, содержащим
хлорид натрия, до 0 °С и медленно при
перемешивании вливают в смесь 600 г льда и 60 см3 концентрированной
серной кислоты, помещенную в стакан вместимостью 2 дм3, охлаждаемый
снаружи смесью льда с хлоридом натрия. Выпавшие кристаллы нитрозометилмочевины
немедленно отфильтровывают на воронке Бюхнера, хорошо отсасывают под вакуумом и
промывают на фильтре ледяной водой.
Внимание! Нитрозометилмочевину хранят в темной
склянке в холодильнике, так как под действием света и
тепла она может взорваться.
7.4. Получение раствора диазометана
Диазометан взрывоопасен и
очень ядовит. Все работы необходимо проводить в вытяжном шкафу!
В коническую колбу на 100 см3
вносят 20 см3 40 %-го раствора гидроксида калия и 50 см3
диэтилового эфира, колбу помещают в баню со льдом и охлаждают до температуры 2
- 5 °С. В охлажденную смесь порциями при перемешивании на магнитной мешалке или
путем встряхивания вносят 5 г нитрозометилмочевины. Реакционную смесь
выдерживают на холоде 10 мин. Затем эфирный слой сливают в чистую коническую
колбу вместимостью 100 см3, добавляют 10 - 15 гранул гидроксида
калия и колбу оставляют в бане со льдом на 2,5 - 3,0 ч для осушения раствора.
Раствор диазометана в эфире
годен к употреблению при хранении в холодильнике в течение 1 - 2 суток. При
хранении сосуды с диазометаном нельзя плотно закрывать!
7.5. Приготовление раствора ортофосфорной
кислоты с массовой долей 0,1 %
(0,1 %-й раствор)
В мерную колбу вместимостью
1000 см3 помещают 250 - 300 м3 бидистиллированной воды,
вносят 1 см3 ортофосфорной кислоты,
доводят водой до метки, перемешивают.
7.6. Приготовление смеси
растворителей для растворения образцов (метод
ВЭЖХ)
В мерную колбу вместимостью
1000 см3 помещают 500 см3 ацетонитрила, вносят 500 см3
0,1 %-го раствора ортофосфорной кислоты, перемешивают, фильтруют через
мембранный фильтр.
7.7. Приготовление градуировочных растворов
7.7.1. Серия № 1
(метод ВЭЖХ)
7.7.1.1.
Исходные растворы биспирибака кислоты, имазапира,
имазетапира, метсульфурон-метила, никосульфурона, пеноксулама, сульфометурон-метила, тифенсульфурон-метила, топрамезона и трифлуфульфурон-метила
для градуировки (концентрация 100 мкг/см3).
В 10 мерных колб вместимостью 100 см3
помещают по 0,0100 г каждого вещества (раздельно), растворяют в 50 - 60 см3
ацетонитрила, доводят ацетонитрилом до метки, тщательно перемешивают.
Растворы хранят в морозильной
камере при температуре -18 °С в течение 3 месяцев.
Растворы № 1 - 5 готовят объемным
методом путем последовательного разбавления исходных растворов для градуировки.
7.7.1.2. Раствор №
1 смеси биспирибака кислоты, имазапира, имазетапира,
метсульфурон-метила, никосульфурона, пеноксулама,
сульфо-метурон-метила, тифенсульфурон-метила,
топрамезона и трифлуфульфурон-метила для градуировки
и внесения (концентрация 10 мкг/см3).
В мерную колбу вместимостью
100 см3 помещают по 10 см3 исходного раствора
каждого вещества с концентрацией 100 мкг/см3 (п. 7.7.1.1), разбавляют ацетонитрилом до метки.
Градуировочный раствор № 1
хранят в морозильной камере при температуре -18 °С в течение месяца.
Этот раствор используют для
приготовления проб с внесением при оценке полноты извлечения веществ методом
«внесено-найдено»,
а также контроле точности измерений методом «добавок».
7.7.1.3. Рабочие растворы №
2 - 5 биспирибака кислоты, имазапира, имазетапира,
метсульфурон-метила, никосульфурона, пеноксулама, сульфометурон-метила, тифенсульфурон-метила, топрамезона
и трифлуфульфурон-метила для градуировки (концентрация
0,05 - 0,5 мкг/см3).
В 4 мерные колбы вместимостью 100 см3
помещают по 0,5; 1,25; 2,5 и 5,0 см3 градуировочного раствора № 1
смеси веществ концентрацией 10 мкг/см3 (п. 7.7.1.2), доводят до метки смесью растворителей,
приготовленной по п. 7.6, тщательно
перемешивают, получают рабочие растворы № 2 - 5 с концентрацией каждого
вещества 0,05; 0,125; 0,25 и 0,5 мкг/см3 соответственно.
Рабочие растворы хранят в
холодильнике при температуре 4 - 6 °С в течение недели.
7.7.2. Серия № 2 (метод
ГЖХ)
7.7.2.1. Исходные
растворы 2,4-Д, МСРА, аминопиралида, ацетохлора,
ацифлуорфена, бентазона, дикамбы, клопиралида и
пиклорама для градуировки (концентрация 200 мкг/см3).
В 9 мерных колб вместимостью 100 см3
помещают по 0,0200 г каждого вещества (раздельно), растворяют в 50 - 60 см3 ацетона,
доводят ацетоном до метки, тщательно перемешивают.
Растворы хранят в морозильной
камере при температуре -18 °С в течение 6 месяцев.
7.7.2.2. Рабочий
раствор № 1 ацетохлора для градуировки (концентрация 1
мкг/см3).
В мерную колбу
вместимостью 100 см3 помещают 0,5 см3 исходного раствора
ацетохлора с концентрацией 200 мкг/см3 (п. 7.7.2.1), разбавляют гексаном до метки.
Градуировочный раствор № 1
хранят в морозильной камере при температуре -18 °С в течение 3 месяцев.
7.7.2.3. Исходный
раствор смеси метиловых эфиров 2,4-Д,
МСРА, аминопиралида, ацифлуорфена, бентазона, дикамбы,
клопиралида и пиклорама для градуировки (соответствует концентрации
2,4-Д, МСРА, аминопиралида, ацифлуорфена,
бентазона, дикамбы, клопиралида и пиклорама 1 мкг/см3).
В круглодонную колбу вместимостью 50 см3 помещают по
0,5 см3 исходного раствора каждого вещества с концентрацией 200
мкг/см3 (п. 7.7.2.1),
растворитель отдувают потоком теплого воздуха, вносят 3 см3 раствора
диазометана, выдерживают 30 мин при комнатной температуре. Для освобождения от
избытка диазометана вносят в колбу 0,1 г
силикагеля, выдерживают еще 15 мин. Затем
добавляют в колбу 0,1 см3 н-пропанола, отдувают растворитель потоком
теплого воздуха (не помещая колбу на подогретую водяную баню) до влажного
остатка. Вносят в колбу 1 см3 гексана и вновь отдувают растворитель
до влажного остатка (отсутствие запаха эфира).
Остаток растворяют в гексане,
перенося порциями растворителя по 10 - 15 см3 в
мерную колбу на 100 см3, доводят
объем до метки, перемешивают.
Раствор смеси метиловых
эфиров веществ с концентрацией 1 мкг/см3 хранят в морозильной камере
при температуре -18 °С в течение месяца.
Растворы № 2 - 5 готовят
объемным методом путем последовательного разбавления исходных растворов.
7.7.2.4. Рабочие
растворы № 2 - 5 смеси метиловых эфиров 2,4-Д, МСРА, аминопиралида,
ацифлуорфена, бентазона, дикамбы, клопиралида, пиклорама,
а также ацетохлора для градуировки (соответствует
концентрации 2,4-Д, МСРА, аминопиралида,
ацетохлора, ацифлуорфена, бентазона, дикамбы, клопиралида
и пиклорама 0,01 - 0,1 мкг/см3).
В 4 мерные колбы вместимостью 100 см3
помещают по 1,0; 2,0; 5,0 и 10,0 см3 исходного раствора смеси
метиловых эфиров 2,4-Д, МСРА, аминопиралида, ацифлуорфена, бентазона, дикамбы, клопиралида, пиклорама (приготовленного по п. 7.7.2.3), а также рабочего раствора № 1 ацетохлора (приготовленного по п. 7.7.2.2), доводят до метки гексаном, тщательно перемешивают,
получают рабочие растворы № 2 - 5 с концентрацией 2,4-Д, МСРА, аминопиралида,
ацетохлора, ацифлуорфена, бентазона, дикамбы, клопиралида и пиклорама 0,01;
0,02; 0,05 и 0,1 мкг/см3 соответственно.
Растворы хранят в морозильной
камере при температуре -18 °С в течение месяца.
7.7.2.5.
Раствор 2,4-Д, МСРА, аминопиралида, ацетохлора,
ацифлуорфена, бентазона, дикамбы, клопиралида и
пиклорама для внесения (концентрация 1 мкг/см3).
В мерную колбу вместимостью
100 см3 помещают по 0,5 см3 исходного раствора каждого
вещества, приготовленного по п. 7.7.2.1,
разбавляют ацетоном до метки.
Раствор хранят в морозильной
камере при температуре -18 °С в течение месяца.
Этот раствор используют для
приготовления проб с внесением при оценке полноты извлечения веществ методом
«внесено-найдено»,
а также контроле точности измерений методом «добавок».
7.8. Установление градуировочных
характеристик
Градуировочные характеристики, выражающие
зависимость площади пика от концентрации биспирибака кислоты, имазапира, имазетапира,
метсульфурон-метила, никосульфурона, пеноксулама,
сульфометурон-метила, тифенсульфурон-метила, топрамезона и
трифлуфульфурон-метила или 2,4-Д, МСРА, аминопиралида, ацетохлора,
ацифлуорфена, бентазона, дикамбы, клопиралида и пиклорама в растворе,
устанавливают методом абсолютной калибровки по 4 растворам для градуировки № 2
- 5 (серия 1 и 2 соответственно).
В инжектор жидкостного хроматографа вводят
по 20 мм3 каждого градуировочного раствора, приготовленного по п. 7.7.1.3, и анализируют в условиях
хроматографирования по п. 7.9.1, в
испаритель газового хроматографа - по 1 мм3 каждого градуировочного
раствора, приготовленного по п. 7.7.2.4,
и анализируют в условиях хроматографирования по п. 7.9.2.1 или 7.9.2.2.
Осуществляют не менее 5 параллельных измерений. Устанавливают площади пиков
веществ (или их метиловых эфиров), на основании которых строят градуировочные
зависимости.
7.9. Условия хроматографирования
7.9.1. Метод ВЭЖХ
Жидкостный хроматограф с быстросканирующим
ультрафиолетовым детектором, снабженный дегазатором, автоматическим
пробоотборником и термостатом колонки.
Рабочие длины волн: 240 и 280
нм (режим сканирования спектров поглощения в диапазоне 190 - 320 нм)*.
__________
* Сканирование поглощения веществ, имеющих специфические
спектры, повышает надежность идентификации.
Хроматографическая колонка
стальная длиной 150 мм, внутренним диаметром 4,6 мм, заполненная
обращенно-фазным сорбентом с привитыми монофункциональными полярными группами С18, зернением 5 мкм.
Температура колонки: 25 °С.
Скорость потока элюента: 0,8
см3/мин.
Объем вводимой пробы: 20 мм3.
Режим элюирования
(градиентный), пробег 32 мин (табл. 5).
Таблица 5
Режим
элюирования
|
Время, мин
|
Содержание растворителя в подвижной фазе, % (по объему)
|
|
ацетонитрил
|
0,1 %-я ортофосфорная кислота
|
|
0,2
|
15
|
85
|
|
0,7
|
30
|
70
|
|
10
|
40
|
60
|
|
13
|
60
|
40
|
|
20
|
70
|
30
|
|
22
|
85
|
15
|
|
26
|
85
|
15
|
|
30
|
15
|
85
|
|
32
|
15
|
85
|
Линейный диапазон
детектирования: 1 - 10 нг.
7.9.2. Метод ГЖХ
7.9.2.1. Газовый
хроматограф, снабженный электронозахватным детектором с пределом детектирования по
линдану 3,4×10-14 г/с, автоматическим пробоотборником,
предназначенный для работы с капиллярной колонкой.
Хроматографическая капиллярная кварцевая
колонка, длиной 30 м, внутренним диаметром 0,25 мм, содержащая сорбент: 14 % цианпропилфенополисилоксана и 86 %
диметилполисилоксана, толщина пленки
сорбента 0,25 мкм.
Температура: детектора 320
°С;
испарителя 240 °С.
Температура термостата колонки
программированная. Начальная температура - 100 °С, выдержка 2 мин, нагрев
колонки со скоростью 8 градусов в минуту до температуры 200 °С, выдержка 5 мин,
нагрев колонки со скоростью 5 градусов в минуту до температуры 260 °С, выдержка
8 мин, нагрев колонки со скоростью 20 градусов в минуту до температуры 280 °С,
выдержка 2 мин.
Газ-носитель - азот, поток 1,0 см3/мин, средняя линейная скорость: 27 см/сек, давление 99,6
кПа.
Хроматографируемый объем: 1
мм3.
Линейный диапазон
детектирования: 0,01 - 0,1 нг.
7.9.2.2.
Газовый хроматограф, снабженный масс-селективным детектором, автоматическим
пробоотборником, предназначенный для работы с капиллярной колонкой.
Хроматографическая капиллярная кварцевая
колонка длиной 30 м, внутренним диаметром 0,25 мм, содержащая сорбент 5 %
фенил- и 95 % диметилполисилоксана, толщина пленки сорбента 0,25 мкм.
Температура: детектора 320 °С;
квадруполя 150 °С, источника
230 °С, переходной камеры 280 °С;
испарителя 250 °С.
Температура термостата колонки
программированная. Начальная температура - 100 °С, выдержка 2 мин, нагрев
колонки со скоростью 5 градусов в минуту до температуры 200 °С, выдержка 5 мин,
нагрев колонки со скоростью 8 градусов в минуту до температуры 260 °С, выдержка
6 мин, нагрев колонки со скоростью 20 градусов в минуту до температуры 300 °С.
Газ 1 (гелий): поток в
колонке 1,3 см3/мин.
Давление: 96,8 кПа.
Средняя линейная скорость: 43
см/с.
Хроматографируемый объем: 1
мм3.
Режим сканирования: SCAN.
Линейный диапазон
детектирования: 0,01 - 0,1 нг.
7.10. Приготовление раствора уксусной
кислоты в воде с массовой долей 1,0 % (1 %-й раствор)
В мерную колбу вместимостью 1000 см3 помещают
250 - 300 м3 бидистиллированной воды, вносят 10 см3
ледяной уксусной кислоты, доводят водой до метки, перемешивают.
Раствор хранят в течение
месяца.
7.11. Приготовление раствора гидроксида
натрия с молярной концентрацией 4 моль/дм3
(4 М раствор)
В мерную колбу вместимостью 250 см3, содержащую 100 - 150 см3 бидистиллированной воды, помещают (40
± 0,1) г натрия гидроксида, доводят водой до метки, тщательно перемешивают.
Раствор хранят в течение
месяца.
7.12. Подготовка концентрирующих
патронов № 1
Патрон устанавливают на аллонж с прямым
отводом для вакуума и промывают последовательно 5 см3 ацетонитрила,
5 см3 бидистиллированной воды, затем 20 см3 1 %-го раствора уксусной кислоты в воде. Скорость потока
растворителей через патрон не должна превышать 2 см3/мин, при этом нельзя
допускать высыхания поверхности патрона. Патрон готовят непосредственно перед
использованием.
7.13. Подготовка концентрирующих
патронов № 2
Патрон устанавливают на
аллонж с прямым отводом для вакуума. Сверху в патрон устанавливают стеклянную
пипетку вместимостью 5 см3, используемую в качестве емкости для
элюента.
Концентрирующий патрон промывают 10 см3
метил-третбутилового эфира, процедуру проводят с использованием вакуума,
скорость потока растворителя через патрон не должна превышать 2 см3/мин, при этом нельзя допускать высыхания поверхности
патрона. Патрон готовят непосредственно перед использованием.
7.14. Подготовка бумажных фильтров для отбора
проб воздуха
Диаметр бумажного фильтра
высокой плотности также должен соответствовать внутреннему диаметру фильтродержателя.
Фильтры последовательно по 3 раза
промывают на воронке Бюхнера этанолом, затем ацетонитрилом порциями 25 - 30 см3,
сушат с помощью разряжения, создаваемого водоструйным насосом, затем на воздухе
при комнатной температуре. До использования фильтры хранят в герметично
закрытой стеклянной таре.
8.1. Вода
Отбор проб производится в соответствии с
правилами, определенными ГОСТ Р 51592-2000 «Вода. Общие
требования к отбору проб», «Унифицированными
правилами отбора проб сельскохозяйственной продукции, продуктов питания и
объектов окружающей среды для определения микроколичеств пестицидов» (от
21.08.79, №
2051-79).
Отобранные пробы воды
отбирают и хранят в стеклянной таре*.
___________
* Использование пластиковой посуды для хранения и
пробоподготовки образцов при применении для
идентификации веществ детектора электронного захвата ионов следует исключить
вследствие возможного загрязнения проб фталатами.
Образцы воды, предназначенные
для определения сульфонил-мочевинных гербицидов (метсульфурон-метил,
никосульфурон, сульфометурон-метил, тифенсульфурон-метил, трифлуфульфурон-метил) хранят в
холодильнике не более суток.
Для дехлорирования воды (при
необходимости) вносят 8 мг тиосульфата натрия (при перемешивании) на 100 см3 образца
воды.
Пробы воды на определение
2,4-Д, МСРА, аминопиралида, ацетохлора, ацифлуорфена, бентазона, дикамбы, клопиралида и
пиклорама, обработанные тиосульфатом натрия, устойчивы при хранении в
холодильнике (4 °С) в темноте в течение 14 дней.
Для длительного хранения
образцы замораживают и хранят при температуре -18 °С.
Перед анализом образцы воды
фильтруют через неплотный бумажный фильтр.
8.2. Атмосферный воздух
Отбор проб осуществляют в
соответствии с требованиями ГОСТ
17.2.4.02-81 «ОПА. Общие требования к методам определения загрязняющих
веществ в воздухе населенных мест».
При измерении концентраций
биспирибака кислоты, имазапира, имазетапира, метсульфурон-метила, никосульфурона, пеноксулама,
сульфометурон-метила, тифенсульфурон-метила, топрамезона и трифлуфульфурон-метила воздух с
объемным расходом 5 дм3/мин
аспирируют через бумажный фильтр высокой плотности, помещенный в
фильтродержатель. Для определения веществ на
уровне предела обнаружения (0,0016 мг/м3)
необходимо отобрать 62,5 дм3 воздуха. Срок хранения отобранных проб,
помещенных в полиэтиленовые пакеты, в морозильной камере при температуре -18 °С
30 дней.
Для установления уровней
2,4-Д, МСРА,
аминопиралида, ацетохлора, ацифлуорфена, бентазона, дикамбы, клопиралида и пиклорама воздух с объемным расходом 2 дм3/мин аспирируют через 2 пробоотборные трубки, установленные
параллельно. Для определения веществ на уровне предела обнаружения (0,00008
мг/м3) необходимо отобрать 125 дм3 воздуха (62,5 дм3
воздуха через каждую трубку). Параллельно экспонированные пробоотборные трубки, герметизированные
заглушками, помещают в полиэтиленовые пакеты попарно. Срок хранения отобранных
проб в холодильнике при температуре 4 °С 14 дней.
8.3. Воздух рабочей зоны
Отбор проб осуществляют в
соответствии с требованиями ГОСТ
12.1.005-88 «ССБТ. Общие санитарно-гигиенические требования к воздуху
рабочей зоны» и Р
2.2.2006-05 (прилож. 9) «Общие методические требования к организации и
проведению контроля содержания вредных веществ в воздухе рабочей зоны», п. 2
«Контроль соответствия максимальным ПДК».
При измерении концентраций
биспирибака кислоты, имазапира, имазетапира, метсульфурон-метила,
никосульфурона, пеноксулама, сульфометурон-метила, тифенсульфурон-метила, топрамезона и
трифлуфульфурон-метила воздух с объемным расходом 2
- 4 дм3/мин аспирируют через бумажный фильтр высокой плотности,
помешенный в фильтродержатель. Для определения
веществ на уровне предела обнаружения (0,25 мг/м3) необходимо отобрать 4 дм3 воздуха. Срок
хранения отобранных проб, помещенных в полиэтиленовые пакеты, в морозильной
камере при температуре -18 °С 30 дней.
Для установления уровней
2,4-Д, МСРА, аминопиралида, ацетохлора, ацифлуорфена, бентазона, дикамбы, клопиралида
и пиклорама воздух с объемным расходом 1 - 2 дм3/мин аспирируют через пробоотборную трубку. Для определения
веществ на уровне предела обнаружения (0,1 мг/м3)
необходимо отобрать 2 дм3 воздуха.
Пробоотборные трубки герметизируют заглушками, хранят в холодильнике при
температуре 4 °С 14 дней.
9.1. Метод ВЭЖХ: биспирибака кислота, имазапир, имазетапир, метсульфурон-метил,
никосульфурон, пеноксулам, сульфометурон-метил,
тифенсульфурон-метил, топрамезон и трифлуфульфурон-метил
9.1.1. Вода
Образец отфильтрованной воды
объемом 200 см3 помещают в плоскодонную колбу вместимостью 250 - 300
см3, доводят рН раствора до 2,5 (контроль по рН-метру) с помощью
ортофосфорной кислоты (85 %-й раствор).
Подготовленную пробу вносят
на концентрирующий патрон № 1, подготовленный по п. 7.12, со скоростью пропускания раствора 2 - 3 капли в
секунду, используя разряжение, создаваемое водоструйным насосом. Элюат
отбрасывают. Высушивают патрон пропусканием воздуха (с использованием вакуума)
в течение 5 мин. Вещества элюируют с патрона 3 см3 ацетонитрила,
собирая элюат в круглодонную колбу для упаривания вместимостью 50 см3.
Растворитель упаривают на ротационном вакуумном испарителе при температуре не
выше 35 °С досуха, остаток растворяют в 2 см3 смеси растворителей,
приготовленной по п. 7.6 и
анализируют при условиях хроматографирования, указанных в п. 7.9.1.
9.1.2. Атмосферный воздух
Экспонированный бумажный
фильтр высокой плотности переносят в химический стакан вместимостью 150 см3,
заливают 20 см3 этанола, помещают на встряхиватель на 10 мин. Растворитель сливают, фильтр
еще дважды обрабатывают новыми порциями этанола объемом 20 см3,
выдерживая на встряхивателе по 10 мин.
Объединенный экстракт
переносят (через воронку) в круглодонную колбу, упаривают на ротационном
вакуумном испарителе при температуре бани
не выше 35 °С почти
досуха, оставшийся растворитель отдувают потоком теплого воздуха. Остаток
растворяют в 2 см3 смеси растворителей, приготовленной по п. 7.6, тщательно перемешивают и
анализируют при условиях хроматографирования, указанных в п. 7.9.1.
9.1.3. Воздух рабочей зоны
Экспонированный бумажный
фильтр высокой плотности переносят в химический стакан вместимостью 150 см3,
заливают 20 см3 этанола, помещают на встряхиватель на 10 мин. Растворитель
сливают, фильтр еще дважды обрабатывают новыми порциями этанола объемом 15 см3,
выдерживая на встряхивателе по 10 мин.
Объединенный экстракт
переносят (через воронку) в мерный цилиндр с пришлифованной пробкой
вместимостью 50 см3, доводят объем до метки этанолом, перемешивают.
Аликвоту раствора объемом 5
см3 (1/10 часть экстракта) переносят с помощью гашетки в
круглодонную колбу на 50 см3, упаривают на ротационном вакуумном
испарителе при температуре бани не выше 35 °С почти досуха, оставшийся
растворитель отдувают потоком теплого воздуха. Остаток растворяют в 2 см3
смеси растворителей, приготовленной по п. 7.6,
тщательно перемешивают и анализируют при условиях хроматографирования,
указанных в п. 7.9.1.
Пробу вводят в инжектор
хроматографа не менее двух раз. Устанавливают площади пиков веществ, с помощью
градуировочных графиков определяют концентрацию в хроматографируемом растворе.
Образцы, дающие пики большие,
чем градуировочный раствор с концентрацией 0,5 мкг/см3, разбавляют
смесью растворителей, приготовленной по п. 7.6 (не более, чем в 50 раз).
9.2. Метод ГЖХ: 2,4-Д,
МСРА, аминопиралид, ацетохлор, ацифлуорфен, бентазона, дикамба, клопиралид и пиклорам
9.2.1. Вода
Образец отфильтрованной воды
объемом 200 см3 помещают в плоскодонную колбу вместимостью 400 - 500
см3, добавляют 4М раствор гидроксида натрия до рН 12 (контроль по индикаторной
бумаге). Оставляют образец на 1 ч при комнатной температуре, периодически
перемешивая.
Доводят рН раствора до 1 с
помощью концентрированной серной кислоты (контроль по индикаторной бумаге).
Непосредственно после подкисления добавляют к раствору 2 г сульфата меди,
перемешивают до полного растворения соли. Цвет водного раствора становится
голубым, что позволяет контролировать распределение водной и органической фаз
при экстракции.
Вносят в раствор 40 г
сульфата натрия (порциями при интенсивном перемешивании до полного растворения
осадка). Вновь контролируют рН раствора (по индикаторной бумаге), при
необходимости доводят рН до 1, используя концентрированную серную кислоту.
Переносят пробу в делительную
воронку вместимостью 500 см3, вносят 75 см3 трет-бутилметилового эфира,
интенсивно встряхивают в течение 3 мин. После полного расслоения фаз верхний
органический слой переносят в круглодонную
колбу для упаривания, фильтруя через слой безводного сульфата натрия (1,5 - 2,0
см), помещенный на бумажном фильтре в химической воронке. Экстракцию повторяют
еще дважды, порциями трет-бутилметилового эфира по 50 см3.
Объединенный экстракт, пропущенный через сульфат натрия, концентрируют на
ротационном вакуумном испарителе при температуре бани не выше 35 °С до влажного
остатка, оставшийся растворитель отдувают потоком теплого воздуха. Для
освобождения от следов воды в колбу вносят 4 - 5 см3 ацетонитрила и
вновь упаривают.
Вносят 2 см3
раствора диазометана, выдерживают 30 мин при комнатной температуре. Для
освобождения от избытка диазометана вносят в колбу 0,1 г силикагеля, выдерживают еще 15 мин. Затем добавляют в колбу 0,1 см3 н-пропанола, отдувают растворитель потоком
теплого воздуха (не помещая колбу на подогретую водяную баню) до влажного
остатка. Вносят в колбу 1 см3 н-гексана и вновь отдувают
растворитель до влажного остатка (отсутствие
запаха эфира).
Остаток растворяют в 3 см3
трет-бутилметилового
эфира, раствор пропускают через концентрирующий патрон № 2, подготовленный по
п. 7.13.
Скорость прохождения раствора через патрон не должна превышать 2 - 3 капли в
секунду. Элюат собирают непосредственно в круглодонную
колбу для упаривания на 50 см3. Патрон дополнительно промывают двумя
порциями трет-бутилметилового эфира объемом 3 см3.
К объединенному элюату в
колбе добавляют 0,1 см3
н-пропанола, отдувают растворитель потоком теплого воздуха (не помещая колбу на
подогретую водяную баню) до влажного остатка. Вносят в колбу 1 см3 н-гексана
и вновь отдувают растворитель до влажного остатка (отсутствие запаха эфира).
Остаток растворяют в 2 см3
гексана и анализируют в условиях хроматографирования, указанных в пп. 7.9.2.1, 7.9.2.2.
9.2.2. Атмосферный воздух
Содержимое 2 экспонированных
пробоотборник
трубок (сорбент и стекловату) переносят в химический стакан вместимостью 100 см3,
заливают 10 см3 ацетона, помещают на ультразвуковую баню на 10 мин.
Растворитель декантируют в круглодонную колбу вместимостью 100 см3 и
повторяют экстракцию новой порцией ацетона объемом 10 см3,
выдерживая на ультразвуковой бане 10 мин.
Объединенный экстракт
переносят (через воронку) в круглодонную колбу, упаривают на ротационном
вакуумном испарителе при температуре бани
не выше 35 °С почти
досуха, оставшийся растворитель отдувают потоком теплого воздуха. Для
освобождения от следов воды в колбу вносят 4 -
5 см3 ацетонитрила и вновь
упаривают.
Вносят 2 см3
раствора диазометана, выдерживают 30 мин при комнатной температуре. Для
освобождения от избытка диазометана вносят в колбу 0,1 г силикагеля, выдерживают еще 15 мин. Затем добавляют в колбу
0,1 см3 н-пропанола, отдувают
растворитель потоком теплого воздуха (не помещая колбу на подогретую водяную
баню) до влажного остатка. Вносят в колбу 1 см3 н-гексана и вновь
отдувают растворитель до влажного остатка (отсутствие запаха эфира).
Остаток растворяют в 2 см3
гексана, тщательно перемешивают и анализируют при условиях хроматографирования,
указанных в пп. 7.9.2.1, 7.9.2.2.
9.2.3. Воздух рабочей зоны
Содержимое пробоотборной трубки (сорбент и
стекловату) переносят в химический стакан вместимостью 100 см3,
заливают 10 см3 ацетона, помещают на ультразвуковую баню на 10 мин.
Растворитель сливают, экстракцию повторяют новой порцией ацетона объемом 10 см3,
выдерживая на ультразвуковой бане 10 мин. Объединенный экстракт переносят
(через воронку) в мерный цилиндр на 25 см3, доводят объем экстракта
до 20 см3 ацетоном, перемешивают.
Аликвоту раствора объемом 2
см3 (1/10
часть экстракта) переносят с помощью пипетки в круглодонную колбу на 50 см3, упаривают на
ротационном вакуумном испарителе при температуре бани не выше 35 °С почти
досуха, оставшийся растворитель отдувают потоком теплого воздуха. Для
освобождения от следов воды в колбу вносят 4 - 5 см3 ацетонитрила и
вновь упаривают.
Вносят 2 см3
раствора диазометана, выдерживают 30 мин при комнатной температуре. Для
освобождения от избытка диазометана вносят в колбу 0,1 г силикагеля, выдерживают
еще 15 мин. Затем добавляют в колбу 0,1 см3
н-пропанола, отдувают растворитель потоком теплого воздуха (не помещая колбу на
подогретую водяную баню) до влажного остатка. Вносят в колбу 1 см3
н-гексана и вновь отдувают растворитель до влажного остатка (отсутствие запаха
эфира).
Остаток растворяют в 2 см3
гексана, тщательно перемешивают и анализируют при условиях хроматографирования,
указанных в пп. 7.9.2.1, 7.9.2.2.
Пробу вводят в испаритель
хроматографа не менее двух раз. Устанавливают площади пиков ацетохлора и
метиловых эфиров веществ, с помощью градуировочных графиков определяют
концентрацию веществ в хроматографируемом растворе.
Образцы, дающие пики большие,
чем градуировочные растворы с концентрацией 0,1 мкг/см3, разбавляют гексаном (не
более, чем в 50 раз).
10.1. Вода
Содержание веществ в пробе
воды (X, мг/дм3) рассчитывают по формуле:
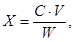 где
где
С - концентрация веществ, найденная по градуировочным
характеристикам в соответствии с величиной площади хроматографического пика,
мкг/см3;
V - объем экстракта, подготовленного для хроматографирования, см3;
W - объем анализируемого образца, см3.
За результат анализа
принимают среднее арифметическое результатов двух параллельных определений,
расхождение между которыми не превышает предел повторяемости:
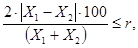 где (1)
где (1)
Х1, Х2 - результаты параллельных определений,
мг/дм3, мг/м3;
r - значение предела повторяемости (табл. 2 - 4), при
этом r = 2,8 ∙ σr.
При невыполнении условия (1) выясняют причины превышения предела
повторяемости, устраняют их и вновь выполняют анализ.
10.2. Воздушная среда
Концентрацию веществ в пробе
атмосферного воздуха или воздуха рабочей зоны (X), мг/м3,
рассчитывают по формуле:
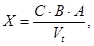 где
где
С - концентрация веществ в
хроматографируемом растворе, найденная по градуировочным характеристикам в
соответствии с величиной площади хроматографического пика, мкг/см3;
В - объем экстракта, подготовленного для хроматографирования, см3;
А - коэффициент, учитывающий аликвотную часть экстракта, взятую для анализа
при исследовании проб воздуха рабочей зоны, равен 10;
Vt - объем пробы воздуха, отобранный для анализа, приведенный к
нормальным условиям при исследовании проб атмосферного воздуха (давление 760 мм
рт.ст., температура 0 °С), стандартным - для воздуха рабочей зоны (давление 760
мм рт.ст., температура 20 °С), дм3:
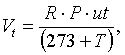 где
где
T - температура воздуха при отборе проб (на
входе в аспиратор), °С;
Р - атмосферное давление при отборе пробы, мм рт.ст.;
и - расход воздуха при отборе пробы, дм3/мин;
t - длительность отбора пробы, мин (при объединении двух
параллельно экспонированных трубок, дополнительно вводится коэффициент 2, т.е. t×2);
R - коэффициент, равный 0,357 для атмосферного воздуха и
0,386 для воздуха рабочей зоны.
Результат анализа
представляют в виде:
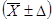 мг/дм3, мг/м3 при вероятности Р
= 0,95, где
мг/дм3, мг/м3 при вероятности Р
= 0,95, где
![]() - среднее арифметическое результатов определений, признанных
приемлемыми, мг/дм3, мг/м3;
- среднее арифметическое результатов определений, признанных
приемлемыми, мг/дм3, мг/м3;
Δ - граница абсолютной погрешности, мг/дм3,
мг/м3:
![]() где
где
δ - граница относительной погрешности
методики (показатель точности по диапазону концентраций, табл. 2 - 4), %.
Если содержание компонента
менее нижней границы диапазона определяемых концентраций, результат анализа
представляют в виде:
«содержание вещества в пробе воды
- менее 0,0001
(0,0005) мг/дм3, атмосферном воздухе
- менее 0,00008 (0,0016) мг/м3, воздухе рабочей зоны
- менее 0,1
(0,25) мг/м3».*
_____________
* - 0,0001 (0,0005) мг/дм3,
0,00008 (0,0016) мг/м3, 0,1 (0,25) мг/м3 -
предел обнаружения веществ в пробах воды, атмосферного воздуха (при отборе 125
или 62,5 дм3 воздуха), воздуха рабочей зоны (при отборе 2 или 4 дм3
воздуха) соответственно.
Оперативный контроль
погрешности и воспроизводимости измерений осуществляется в соответствии с ГОСТ
Р ИСО 5725-(1
- 6)-02 «Точность (правильность и
прецизионность) методов и результатов измерений».
12.1. Контроль стабильности
градуировочной характеристики
Контроль стабильности
градуировочной характеристики проводят в начале и по окончании каждой серии
анализов.
При контроле стабильности
градуировочной характеристики проводят измерения не менее трех концентраций
образцов для градуировки, содержание веществ в которых должно охватывать весь
диапазон концентраций от 0,05 до 0,5 мкг/см3 (метод ВЭЖХ) и от 0,01
до 0,1 мкг/см3 (метод ГЖХ).
Градуировочная характеристика
считается стабильной, если для каждого из используемого для контроля
градуировочного раствора сохраняется соотношение:
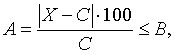 где
где
X - концентрация вещества в пробе при контрольном измерении,
мкг/см3;
С - известная концентрация градуировочного раствора вещества, взятая
для контроля стабильности градуировочной характеристики, мкг/см3;
В - норматив контроля погрешности градуировочной характеристики, %
(равен 10 % при Р = 0,95).
Если величина расхождения (А) превышает 10 %-ю погрешность
градуировочной характеристики, делают вывод о невозможности применения
градуировочной
характеристики для дальнейших измерений. В этом случае выясняют и устраняют
причины нестабильности градуировочной характеристики и повторяют контроль ее
стабильности с использованием других градуировочных растворов веществ,
предусмотренных МВИ. При повторном обнаружении нестабильности градуировочной
характеристики устанавливают ее заново согласно п. 7.8.
Стабильность результатов
измерений контролируют перед проведением измерений, анализируя один из
градуировочных растворов.
12.2. Плановый внутрилабораторный оперативный контроль процедуры
выполнения анализа проводится методом «добавок»
Образцами для контроля
являются реальные пробы водной и воздушной сред. Объем отобранных для контроля
процедуры выполнения анализа проб воды и воздуха должен соответствовать
удвоенному объему, необходимому для проведения анализа по методике.
При исследовании проб
воздушной среды экстракт с фильтра (или сорбционной трубки) делят на две равные части, первую из которых
анализируют в точном соответствии с прописью методики и получают результат
анализа исходной рабочей пробы - X. Во вторую
часть делают добавку анализируемого компонента (Сд) и анализируют в точном соответствии с прописью методики, получая
результат анализа рабочей пробы с добавкой - X'. Результаты анализа исходной рабочей пробы (X) и рабочей пробы с добавкой (X') получают в условиях повторяемости (один
аналитик, использование одного набора мерной посуды, одной партии реактивов и т.д.).
Величина добавки Сд должна
удовлетворять условию:
 где
где
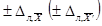 - характеристика погрешности (абсолютная погрешность)
результатов анализа, соответствующая содержанию компонента в испытуемом образце
(расчетному значению содержания компонента в образце с добавкой
соответственно), мг/дм3 мг/м3,
- характеристика погрешности (абсолютная погрешность)
результатов анализа, соответствующая содержанию компонента в испытуемом образце
(расчетному значению содержания компонента в образце с добавкой
соответственно), мг/дм3 мг/м3,
при этом:
Δл = ±0,84Δ, где
Δ - граница абсолютной погрешности, мг/ дм3,
мг/м3:
![]() где
где
δ - граница относительной погрешности
методики (показатель точности в соответствии с диапазоном концентраций, табл. 2 - 4), %.
Результат контроля процедуры Кк рассчитывают по формуле:
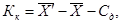 где
где
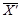 ,
, ![]() , Сд - среднее значение массовой концентрации вещества в образце с добавкой,
испытуемом образце, концентрация добавки соответственно, мг/дм3, мг/м3.
, Сд - среднее значение массовой концентрации вещества в образце с добавкой,
испытуемом образце, концентрация добавки соответственно, мг/дм3, мг/м3.
Норматив оперативного
контроля точности К рассчитывают по формуле:
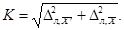
Проводят сопоставление
результата контроля процедуры (Кк) с нормативом контроля (К).
Если результат контроля
процедуры удовлетворяет условию
|Кк|
≤ К, (2)
процедуру анализа признают
удовлетворительной.
При невыполнении условия (2) процедуру контроля повторяют. При
повторном невыполнении условия (2)
выясняют причины, приводящие к неудовлетворительным результатам, и принимают
меры по их устранению.
12.3. Проверка приемлемости
результатов измерений, полученных в условиях
воспроизводимости
Расхождение между
результатами измерений, выполненных в условиях воспроизводимости (разное время,
разные операторы, разные лаборатории), не должно превышать предел
воспроизводимости (R):
 где (3)
где (3)
Х1, Х2 - результаты измерений, выполненных в условиях
воспроизводимости (разное время, разные операторы, разные лаборатории), мг/дм3,
мг/м3;
R - предел воспроизводимости (в соответствии с диапазоном
концентраций, табл. 2), %.
Если выполняется условие (3), то воспроизводимость измерений
считается удовлетворительной.
При превышении норматива
контроля воспроизводимости эксперимент повторяют, при повторном превышении
указанного норматива выясняют причины и по возможности их устраняют.
Новости
Библиотека
Soft по ОТ и ПБ
Консультации по ОТ
Обучение по охране труда и пр.
Услуги для ОТ
Форум
Золотой фонд
Соцсеть специалистов (ССОТ)






